Régénération parodontale : Entire Papilla Regeneration Technique (EPPT)
Le but du traitement chirurgical d’un défaut parodontal intra-osseux est d’obtenir la régénération de l’ensemble du parodonte. A ce titre, la régénération tissulaire guidée (GTR) a démontré de meilleurs résultats en termes de réduction de profondeur de poche et de gain d’attache1 par rapport à un débridement par lambeau d’accès. Néanmoins, c’est une technique qui présente un taux de morbidité élevé, jusqu’à 50% de réouverture du site lors de la cicatrisation2. Dans ces cas-là, l’exposition des membranes et leur contamination par des bactéries peut compromettre la régénération tissulaire3,4 et induire des modifications macroscopiques de l’architecture tissulaire5.
En 1997, Heijl6 démontre que l’application topique de dérivés de la matrice amélaire (EMD) sur une surface radiculaire propre et en regard d’un défaut intra-osseux permet de promouvoir le gain d’attache clinique et la formation d’os objectivée radiographiquement. La validation de l’utilisation de l’EMD7,8 fait évoluer la régénération tissulaire guidée alors caractérisée par l’utilisation de membranes, et dont la mise en place nécessite la réalisation d’accès chirurgicaux étendus, à une régénération tissulaire induite. Dans cette approche, la stabilité du caillot de sang est recherchée par une chirurgie a minima et l’utilisation de matériaux de comblement en tant que mainteneurs d’espace et soutiens physiques si nécessaire.
Ainsi, de nombreux tracés de lambeaux sont proposés fin des années 90. On peut citer à titre d’exemples les approches de Cortellini et al. décrites en 1995 et 1999 respectivement : le Modified Papilla Preservation Flap9 (MPPF) et le Simplified Papilla Preservation Flap10 (SPPF) indiqués selon que l’espace proximal en regard de la lésion intra-osseuse est >2mm ou <2mm. Ces designs ont permis de faire chuter le taux de réouverture des lambeaux à 30%10,11. Ce pourcentage va à nouveau réduire pour atteindre 10% lorsque ces lambeaux sont combinés à une élévation chirurgicale papillaire a minima et sélectionnée selon l’étendue vestibulo-proximo-linguale de la lésion intra-osseuse12,13.
Récemment, Aslan et al. ont présenté l’Entire Papilla Preservation Technique14 (EPPT) dont le but est de régénérer une lésion intra-osseuse tout en réduisant d’avantage le taux de complications post-opératoire de type réouverture de lambeau et apparition de déhiscences tissulaires.
Cet article propose de décrire la technique chirurgicale présentée par l’équipe d’Aslan, d’en préciser les indications et les limites.
Rapport de cas
Une patiente de 25 ans est adressée au cabinet après 6 mois de traitement parodontal non chirurgical pour prise en charge d’une lésion intra-osseuse en mésial de 33. La patiente est non fumeuse, ne présente pas d’allergies ou de carences et ne suit aucun traitement médicamenteux.
L’examen clinique montre les éléments suivants :
- absence d’inflammation ;
- présence discrète de plaque, quasi nulle ;
- phénotype épais ;
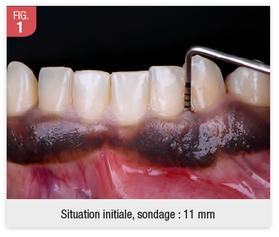
- profondeur de sondage en mésial de 33 : 11mm (Fig.1) ;
- gingivorragie au sondage.
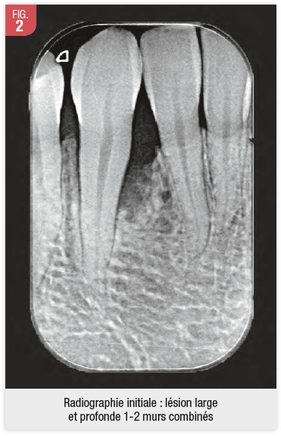
L’examen radiographique montre les éléments suivant (Fig.2) :
- lésion intra-osseuse en mésial de 33 ;
- présence d’un mur osseux lingual.
Préalablement à l’intervention, il demandé à la patiente de démarrer une antibiothérapie (Amoxicilline 0.5gr 3 fois par jour, 6 jours) et une corticothérapie (Prednisolone 60mg en prise unique le matin, 4jours) à partir de la veille de l’intervention.
Chirurgie
Anesthésie
L’anesthésie (Chlorhydrate d’Articaïne adrénaliné 1/100000) est réalisée à distance du site opératoire pour limiter les microperforations de la muqueuse.
Accès
Selon la technique décrite par Aslan et col., le lambeau d’accès est réalisé de la façon suivante :
- incision intrasulculaire (Viper, MJK) en 32 et 33; (Fig.3)
- incision verticale de décharge biseautée (lame 15C) depuis le collet jusqu’à la ligne muco-gingivale et élévation de la totalité du tissu proximal papillaire supra-crestal à l’aide de couteaux à tunnéliser (TKN1, TKN2, Hu-Friedy) assurant l’accès à l’espace proximal et à la lésion ; (Fig.4)
la technique initiale ne propose pas de réaliser des incisions dans différents plans au-delà de la ligne muco-gingivale. Néanmoins, compte-tenu du phénotype épais, nous avons réalisé une incision partielle superficielle pour libérer la muqueuse et gagner en laxité (Fig.5).




Curetage, préparation radiculaire, comblement
Le tissu de granulation de la composante intra-osseuse de la lésion est éliminé à l’aide de micro-excavateurs, le but étant d’obtenir les conditions suffisantes pour l’application de l’EMD sur les racines qui doit se faire en l’absence de saignements.
La surface radiculaire est instrumentée à l’aide d’ultrasons et de micro-curettes.
Un gel d’EDTA 24% (Prefgel, Straumann) est mis en place sur la racine pendant 2 minutes puis rincé abondement pendant 1 minute par de la solution saline.
L’EMD (Emdogain, Straumann) est ensuite appliqué sur la racine.
Enfin, dans ce cas spécifiquement la fraction intra-osseuse de la lésion parodontale est large et profonde (>5mm de sondage). Un matériau de comblement allogénique (CS fine, Allodyn) est mis en place pour favoriser la stabilité du caillot de sang et soutenir les tissus mous (Fig. 6).

Sutures
Le lambeau est suturé sans tension à l’aide d’un fil non résorbable en polypropylène 6-0. Des nœuds simples en « o » sont réalisés en faisant attention de repositionner précisément les berges (Fig. 7)
Conseils post-opératoires
Il est demandé à la patiente d’éviter tout brossage pendant 10 jours jusqu’à la dépose des sutures, après cette durée elle utilisera une brosse à dent 7/100e pendant à nouveau 10 jours avant de reprendre une routine classique.
En cas de douleurs, du paracétamol (1gr toutes les 6 heures sans dépasser 3gr/jour) est prescrit.
Il lui est demandé de pulvériser un gel d’acide hyaluronique (Hyalugel spray Forte) toutes les 6 heures pendant 6 jours.
Dépose des sutures : 10 jours post-opératoires
Lors du rendez-vous de dépose des sutures, l’examen clinique montre les éléments suivants :
- absence d’ouverture du lambeau ;
- présence de plaque en rapport avec l’absence de brossage et inflammation discrète.
La patiente ne rapporte aucune douleurs ou inconfort, les sutures sont déposées à l’aide de micro-ciseaux et une brossette et de la pâte à polir sont utilisées pour éliminer la plaque.

Discussion
Les résultats présentés dans ce rapport de cas sont comparables avec ceux rapportés par Aslan et al. dans des situations similaires de lésions intra-osseuses de 1-2 murs osseux. En réalisant l’EPPT seule, sans biomatériaux de comblement, Aslan15 montre une réduction moyenne de profondeur de poche de 6,2+/-1,33mm et un gain d’attache moyen de 5,83+/-1,12mm. Pour le cas présenté, un biomatériau de comblement a été utilisé selon les recommandations de Santoro et al.16 en présence d’une lésion intra-osseuse >5mm de profondeur. Le but étant de soutenir les tissus et de favoriser la stabilisation du caillot de sang et donc d’optimiser le processus de régénération. Néanmoins, les résultats d’Aslan, en combinant EPPT, EMD et biomatériaux, sont similaires en termes de gain d’attache clinique et de réduction de profondeur de sondage : 6,5+/-2,65mm et 6,3+/-2,5mm15 respectivement, à ceux obtenus avec l’EPPT seule. Ces résultats à 1 an suggèrent donc que l’utilisation d’EMD et de comblement n’apporte rien à l’EPPT et pourrait être évitée. Pourtant, la topographie des lésions, l’angle osseux ou le phénotype tissulaire ne sont pas pris en compte dans la présentation de ces résultats. L’EPPT est associée à un pourcentage nul de réouverture du lambeau même lorsqu’une membrane est utilisée15,17, un biomatériau dont le rôle est de soutenir les tissus peut donc être utilisé sans risques jusqu’à précision ultérieure de l’influence réelle sur les performances de l’EPPT seule des paramètres mentionnés précédemment.
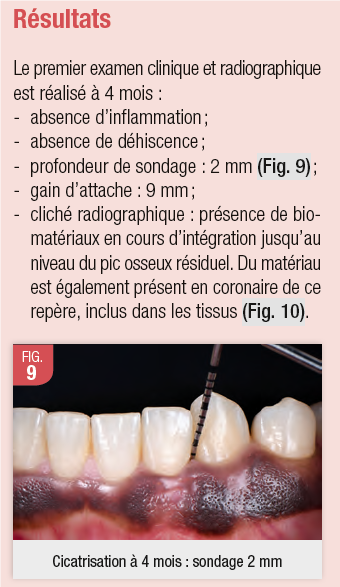
La radiographie à 4 mois montre la fraction supra-crestale du biomatériau de comblement. Compte-tenu de la position du pic osseux, il est improbable que cette fraction régénère de l’os. Néanmoins, l’inclusion de ce biomatériau en transmuqueux sans inflammation a été précédemment décrite par Cardaropoli18 puis Chu19 dans le cadre de la Dual-zone. C’est donc un événement sans conséquences négatives a priori et dont l’impact sur l’amélioration de la qualité des tissus mous reste inexploré dans le cadre de la régénération parodontale bien que décrit en implantologie. L’avantage majeur de cette technique réside dans son tracé d’incision qui laisse la papille et le tissu proximal supra-crestal intacts. Le maintien d’une importante vascularisation proximale et du tissus proximal semble favoriser la cicatrisation à court terme : un taux de réouverture du lambeau de 0%15,17 est ce jour associé à l’EPPT, mais également à long terme puisque les valeurs de déhiscences vestibulaires à 1 an sont comprises entre 0,2+/-0,25mm et 0,36+/-0,54mm15.
A contrario, ce même design limite l’utilisation de l’EPPT dont l’accès ne permettra pas l’instrumentation de la totalité de la lésion en cas d’étendue linguale importante. De plus, en présence d’une récession vestibulaire associée à la lésion proximale, l’EPPT ne permettra de traiter que la lésion intra-osseuse sans recouvrement radiculaire.
Conclusion
L’Entire Papilla Preservation Technique proposée par Aslan et al. depuis 2017 est une technique séduisante, associée à d’excellents résultats cliniques de gain d’attache et de réduction de profondeur de sondage dans le cadre du traitement chirurgical de lésion intra-osseuses de 1-2 murs combinés sans étendue linguale excessive. Ce jour, les taux de réouverture du lambeau en post-opératoire sont nuls, ce qui en fait une technique de choix en régénération parodontale.
Bibliographie
- Needleman I, Worthington HV, Giedrys-Leeper E, Tucker R. WITHDRAWN: Guided tissue regeneration for periodontal infra-bony defects. Cochrane Database Syst Rev. 2019 May 29;5(5):CD001724.
- De Sanctis M, Zucchelli G, Clauser C. Bacterial colonization of barrier material and periodontal regeneration. J Clin Periodontol 1996;23:1039–1046.
- Nowzari H, Matian F, Slots J. Periodontal pathogens on polytetrafluoroethylene membrane for guided tissue regeneration inhibit healing. J Clin Periodontol 1995;22:469–474.
- De Sanctis M, Zucchelli G, Clauser C. Bacterial colonization of barrier material and periodontal regeneration. J Clin Periodontol 1996;23:1039–1046.
- Machtei EE, Cho MI, Dunford R, Nor- deryd J, Zambon JJ, Genco RJ. Clinical, microbiological, and histological factors which influence the success of regenerative periodontal therapy. J Periodontol 1994;65:154–161.
- Heijl L, Heden G, Svärdström G, Ostgren A. Enamel matrix derivative (EMDOGAIN) in the treatment of intrabony periodontal defects. J Clin Periodontol. 1997 Sep;24(9 Pt 2):705-14.
- Pontoriero R, Wennström J, Lindhe J. The use of barrier membranes and enamel matrix proteins in the treatment of angular bone defects. A prospective controlled clinical study. J Clin Periodon- tol 1999;26:833–840.
- Sculean A, Windisch P, Chiantella GC, Donos N, Brecx M, Reich E. Treatment of intrabony defects with enamel matrix proteins and guided tissue regeneration. A prospective controlled clinical study. J Clin Periodontol 2001;28:397–403
- Sculean A, Schwarz F, Miliauskaite A, et al. Treatment of intrabony defects with an enamel matrix protein derivative or bioabsorbable membrane: An 8-year follow-up split-mouth study. J Periodon- tol 2006;77:1879–1886.
- Cortellini P, Prato GP, Tonetti MS. The modified papilla preservation technique. A new surgical approach for interproximal regenerative procedures. J Periodontol. 1995 Apr;66(4):261-6.
- Cortellini P, Prato GP, Tonetti MS. The simplified papilla preservation flap. A novel surgical approach for the management of soft tissues in regenerative procedures. Int J Periodontics Restorative Dent. 1999 Dec;19(6):589-99.
- Cortellini P, Tonetti MS. A minimally invasive surgical technique with an enamel matrix derivative in the regenerative treatment of intra-bony defects: a novel approach to limit morbidity. J Clin Periodontol. 2007 Jan;34(1):87-93.
- Cortellini P, Tonetti MS. Improved wound stability with a modified minimally invasive surgical technique in the regenerative treatment of isolated interdental intrabony defects. J Clin Periodontol. 2009 Feb;36(2):157-63.
- Aslan S, Buduneli N, Cortellini P. Entire Papilla Preservation Technique: A Novel Surgical Approach for Regenerative Treatment of Deep and Wide Intrabony Defects. Int J Periodontics Restorative Dent. 2017 Mar/Apr;37(2):227-233.
- Aslan S, Buduneli N, Cortellini P. Clinical outcomes of the entire papilla preservation technique with and without biomaterials in the treatment of isolated intrabony defects: A randomized controlled clinical trial. J Clin Periodontol. 2020 Apr;47(4):470-478.
- Santoro G, Zucchelli G, Gherlone E. Combined Regenerative and Mucogingival Treatment of Deep Intrabony Defects Associated with Buccal Gingival Recession: Two Case Reports. Int J Periodontics Restorative Dent. 2016 Nov/Dec;36(6):849-857.
- Aslan S, Buduneli N, Cortellini P. Reconstructive surgical treatment of isolated deep intrabony defects with guided tissue regeneration using entire papilla preservation technique: A prospective case series. J Periodontol. 2021 Apr;92(4):488-495.
- Cardaropoli D, Tamagnone L, Roffredo A, Gaveglio L, Cardaropoli G. Socket preservation using bovine bone mineral and collagen membrane: a randomized controlled clinical trial with histologic analysis. Int J Periodontics Restorative Dent. 2012 Aug;32(4):421-30. PMID: 22577648.
- Chu SJ, Salama MA, Salama H, Garber DA, Saito H, Sarnachiaro GO, Tarnow DP. The dual-zone therapeutic concept of managing immediate implant placement and provisional restoration in anterior extraction sockets. Compend Contin Educ Dent. 2012 Jul-Aug;33(7):524-32, 534. PMID: 22908601.
Retour au dossier Chirurgie parodontale autour des dents et des implants AON #53 - Oct 2022
