Prix Breillat 2016
Prévalence et conséquences de l’hypovitaminose D : pandémie à répercussions bucco-dentaires
Lauréate : Elisa CHOUKROUN
Faculté : Nice
Directeur de thèse : Dr Catherine Pesci-Bardon

La dentisterie moderne tend petit à petit à s’intéresser à l’état biologique et physiologique du patient, dans le but d’une approche globale et médicale. Parmi les facteurs influents sur la santé et le bien être en général, la vitamine D suscite un intérêt croissant pour le tropisme de son action. On compte près de 13 000 articles publiés à ce sujet, rien que ces trois dernières années. En effet, de nombreux articles relatent son rôle crucial dans le métabolisme osseux mais également dans d’autres affections, immunitaires, allergiques, cancéreuses ou encore cérébrales. Cette hormone clé de la « bonne santé » interagit aussi sur la sphère orale (1).
La vitamine D : Description et métabolisme
La vitamine D fait parler d’elle pour la première fois au 20ème siècle pour son implication dans la survenue du rachitisme. C’est en réalité une hormone de la famille des stéroïdes et non une vitamine au sens propre. On la retrouve sous 2 formes inertes, biologiquement équivalentes :
- la vitamine D2, aussi appelée ergocalciférol, d’origine végétale,
- la vitamine D3, ou cholécalciférol d’origine alimentaire ou synthétisée après exposition solaire.
Sources
La vitamine D a donc plusieurs origines possibles.
- L’exposition solaire : sous l’action des rayonnements UVB (290 à 315nm), la vitamine D est produite par les couches profondes de l’épiderme. Cette source constitue la voie principale de synthèse avec 80 à 90% des apports.
- L’alimentation : très peu d’aliments contiennent naturellement de la vitamine D. On retrouve surtout les poissons gras (de préférence sauvages) et les œufs. Pour contrer cela, des nombreux produits laitiers sont maintenant enrichis en vitamine D comme le lait ou les yaourts.
- Une supplémentation sous forme de compléments alimentaires est également une source fiable de vitamine D.
Métabolisme
L’exposition aux rayons UVB permet la conversion du 7-déhydrocholestérol en pré-vitamine D puis rapidement en vitamine D.
Dans le foie, elle subit une autre transformation en 25-hydroxy-vitamine D, qu’on appelle aussi calcifédiol. C’est cette forme qui est analysée lors des prélèvements sanguins en laboratoire.
La 25-hydroxy-vitamine-D va subir une deuxième hydroxylation en 1,25-di-hydroxy-vitamine D, ou calcitriol, au niveau des reins. Cette dernière étape est régulée par la parathormone (PTH), mais aussi par la phosphorémie et la calcémie.
La vitamine D, sous toute ses formes, va ensuite agir sur l’ensemble des tissus via son récepteur cellulaire le VDR (Vitamine D Receptor), présent aussi bien au niveau du tissu osseux, que de la peau, des intestins, du système immunitaire ou encore du tissu cérébral.
Dosage et taux physiologiques
Les ANC, décrétés par les autorités sanitaires françaises, sont de 200 UI par jour pour les adultes et adolescents et 400 UI pour les enfants et personnes âgées. Quant aux différents statuts vitaminiques, le consensus international est le suivant :
-0-5ng/ml – 0-15nmol/ml : carence sévère
-5-10 ng/ml ou 15-25nmol/ml : carence
-10-30 ng/ml ou 25-75nmol/ml : déficience
-> 30 ng/ml ou 75nmol/ml : optimal
-> 150ng/ml: toxicité
Le taux optimal est donc de 30ng/ml. Ce dernier peut être élevé à 50ng/ml en cas de pathologies telles que le cancer (2). Un surdosage en vitamine D reste un phénomène exceptionnel. En cas de taux élevé, les excès sont convertis et excrétés au niveau du rein, limitant la toxicité et la rendant rare. Des études ont démontré que cette dernière n’est toujours pas atteinte pour des doses quotidiennes même 8 fois supérieures aux ANC (3).
Hypovitaminose D : facteurs de risque, épidémiologie & étude
Facteurs de risque
Les facteurs de risques de l’hypovitaminose D sont multiples et variés.
- Âge : En effet les personnes âgées ne conservent que 25% de leur capacité de production de vitamine D, par une baisse de la production de 7-déhydrocholestérol et une exposition réduite. Les nourrissons sont aussi des individus à risques, particulièrement en cas d’allaitement maternel.
- Femmes enceintes : déficitaires à hauteur de 76%
- Couleur de peau : la mélanine rentre en compétition avec le 7-déhudrocholestérol pour l’absorption des UVB. Les personnes de couleur requièrent ainsi une exposition 5 à 10 fois supérieure pour la même quantité de vitamine D synthétisée
- Obésité : la vitamine D étant liposoluble, sa mise à disposition est difficile chez les personnes obèses, qui doivent en consommer 2 à 5 fois plus qu’une personne de poids normal pour maintenir des taux adéquats
- Pathologies digestives malabsorbtives et certains traitements médicamenteux (AIS, anti convulsionnant, VIH…)
- Situation géographique : les personnes habitant à des latitudes supérieures à + ou - 35°, perçoivent moins d’UVB à cause de l’incidence de ces rayons
- Crème solaire : réduit la production de 95% de la vitamine D
- Mode de vie : vêtements, fenêtres….
Epidémiologie
Selon certains spécialistes de la vitamine D, la situation mondiale est qualifiée de « pandémique » (4,5). L’enquête SUVIMAX, menée en France en 2011, recense 78% de patients déficitaires, avec une atteinte plus marquée du sexe féminin (6).
D’autres études (7) estiment à 73% le taux de la population avec un taux inférieur à 20ng/ml en hiver.
Parmi les populations à risque, 100% des personnes institutionnalisées seraient déficitaires.
Étude
Aux vues de ces résultats, nous avons souhaité connaître l’état vitaminique de nos patients.
Méthode
Nous avons testé 3 populations distinctes :
- La première (série 1) regroupe 304 patients examinés dans le cadre d’une consultation pré-implantaire dans 2 cabinets privés spécialisés en implantologie en France (Dr Khoury, Paris et Dr Russe, Reims). La moyenne d’âge est de 63,4 ans ± 8,48 ans.
- La série 2 concerne 48 patients atteints de cancers oro-faciaux en attente de chirurgie carcinologique, suivis dans le service de chirurgie maxillo-facial à l’hôpital universitaire de Francfort sur le Main (Allemagne). L’âge moyen est de 63 ans ± 13,75 ans.
- Le 3ème groupe (série 3) est constitué par le personnel médical du même hôpital (Francfort sur le Main), soit 24 adultes de 49,8 ans en moyenne ± 21,16 ans
Résultats
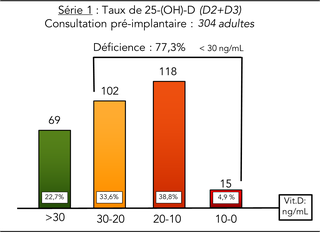
Série 1 : sur un total de 304 patients, seuls 69, soit 22,7% ont un taux adéquat de vitamine D, supérieur à 30ng/ml. 77,3% ont donc un taux insuffisant avec 4,9% de carencés (taux en dessous de 10ng/ml).
Fig. 1 : dosage de la vitamine D chez des patients se présentant à une consultation pré implantaire
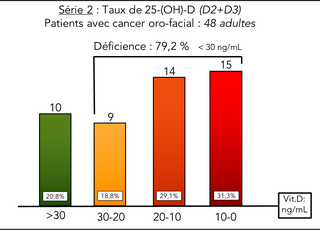
Série 2 : le pourcentage de patients avec un taux inadéquat est semblable à la série 1, avec 79,2% de la population étudiée. Mais les patients cancéreux sont plus sévèrement touchés. En effet, 31,3% des patients sont en état de carence.
Fig. 2 : dosage de la vitamine D chez des patients se présentant à une consultation pré opératoire en cancérologie maxillo-faciale
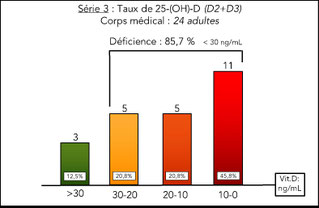
Série 3 : le personnel médical soignant est tout aussi déficitaire que la population générale. Cependant le nombre de carencés est extrêmement élevé : 45,8%. Seuls 3 patients sur 24 soit 12,5% ont un taux de vitamine D supérieur à la valeur seuil de 30 ng/mL.
Fig. 3 : dosage de la vitamine D chez médecins et chirurgiens traitants hospitaliers
Discussion
Concernant les patients examinés en pré-implantaire, les données correspondent à la population générale avec 78,2% de déficients en vitamine D. En effet, ces personnes sont considérées comme globalement en bonne santé car non contre-indiquées à une chirurgie implantaire. Ces données correspondent à celles de la littérature. La population cancéreuse, elle, est plus gravement déficitaire que la population dite classique. Cela correspond également aux dernières données de la littérature qui ont démontré l’aspect protecteur de la vitamine D contre plusieurs types de cancer (8, 9,10).
Mais les personnes les plus carencées sont retrouvées parmi le personnel médical : plus de 45% du corps médical testé est carencé avec un taux inférieur à 10ng/ml. Ce nombre très élevé peut-être expliqué par un défaut de prise de conscience du corps médical ainsi que le rythme de vie et le volume horaire des journées de travail, sans voir la lumière du jour. Les médecins supplémentent leurs patients mais ne se sentent souvent que très peu concernés par le problème.
Certes l’étude n’est pour l’instant qu’à son début. Les groupes restent inégaux et la différence de localisation des patients peut influer sur l’ensoleillement et la déficience, même si ces villes se trouvent à des latitudes proches. Il sera nécessaire de la continuer dans le temps afin d’obtenir des séries plus homogènes.
Conséquences d’une déficience en vitamine D
Conséquences générales
Immunité
Depuis l’article de P. Liu dans Science (11), nous savons maintenant que la vitamine D est un immuno-modulateur naturel. En effet, face à la présence de micro-organismes dans le corps humain, une réponse immunitaire se met en place : les lymphocytes vont initier une cascade de réactions aboutissant à la production de substances anti bactériennes humaines (types cathélicidine ou défensine). Mais cette réponse ne peut se faire qu’en présence d’un taux adéquat de vitamine D. Cette dernière est donc essentielle à un système immunitaire compétent.
Les conséquences d’une carence sont donc les suivantes.
- Moindre résistance aux infections respiratoires (ex : tuberculose), virales ou nosocomiales (12)
- Augmentation du risque de maladies auto-immunes (ex : scléroses-en-plaque, polyarthrite rhumatoïde, lupus érythémateux, maladie de Crohn) (13)
- Augmentation de 200% du risque de diabète de type 1, d’après une puissante étude finlandaise portant sur 10 000 nouveau-nés sur plus de 30 ans (14)
Cancer
Le cancer a souvent été décrit comme touchant d’avantage l’hémisphère nord car moins exposé au rayonnement solaire. Or ce n’est que récemment que le lien avec la vitamine D a été soulevé. A présent, 10 000 articles traitent de ce sujet. La vitamine D régulerait un certain nombre de gènes contrôlant la prolifération et la différenciation des cellules malignes (15, 16, 17,18).
Une hypovitaminose D est associée à :
- une augmentation de 30 à 50% de la prévalence de 13 types de cancers différents en cas de taux inférieurs à 20 ng/ml (contre les 30 ng/ml requis). Ce risque passe à 253% en cas de carence sous 12 ng/ml.
- l’accélération de l’apparition des cancers de 3 à 5 ans (19)
- 21 000 décès annuels en Grande Bretagne, tous cancers confondus, qui découleraient directement d’une défaillance en vitamine D (20).
Système neurologique
Le récepteur de la vitamine D est largement retrouvé au niveau des tissus cérébraux. Il permet ainsi une protection du système nerveux central via l’homéostasie phospho-calcique. Un taux inadéquat de vitamine D a donc les conséquences suivantes :
- incidence augmentée de dépression, schizophrénie et troubles du développement (21)
- risque augmenté de démence de 20% (22)
- facteur de risque de la maladie d’Alzheimer, de la maladie de Parkinson (23)
Systèmes cardio vasculaire et pulmonaire
La vitamine D influerait sur la production de l’angiotensine via le contrôle du gène de la rénine. Les études sont encore peu nombreuses dans ces domaines mais certaines pistes se démarquent :
- augmentation du risque d’hypertension (24)
- augmentation du risque d’angor (25)
- diminution de la capacité pulmonaire (26,27)
- augmentation du risque de la survenue d’asthme de 89% (26)
Métabolisme lipidique
Nous l’avons vu, vitamine D et cholestérol partage le même précurseur, le 7-dehydrocholesterol. En cas d’insuffisance en vitamine D, nous avons donc :
- multiplication du risque de défaillance lipidique par 4
- augmentation de l’incidence du diabète de type 2 de 33% (28)
Les 2 métabolismes sont donc intimement liés. En effet, supplémenter un patient en vitamine D permet de réduire son taux de LDL cholestérol et l’apport de statines (traitement de choix du cholestérol) permet d’augmenter le taux circulant de vitamine D (29). Dans notre étude nous avons également testé le cholestérol des patients. 63,8 % des patients déficitaires en vitamine D présente une hypercholestérolémie.
Fonction musculaire et douleurs
Les douleurs et faiblesse musculaires sont des conséquences fréquentes de l’ostéomalacie.
On retrouve de nombreux récepteurs de la vitamine D dans le tissu musculaire, nécessaires à son activation. En cas d’hypovitaminose D, on retrouve :
- augmentation du risque de chute de 22% et jusqu’à 72% pour les personnes âgées institutionnalisées (30
- diminution des capacités physiques (31)
- augmentation des douleurs musculaires et osseuses diffuses non spécifiques (32)
La vitamine D, ou plutôt son manque, est donc un facteur de co-morbidité mais également un facteur à haut risque de mortalité, en particuliers pour les populations les plus âgées. Elle représenterait 60 à 70% de la mortalité des pays développés, toutes affections confondues (cancer, diabète, maladies cardio-vasculaires etc...)
Conséquences bucco dentaires
Métabolisme osseux
L’impact osseux de la vitamine D est l’un des plus documenté. Le VDR (récepteur de la vitamine D), activé au sein des ostéoblastes stimule la production de Rank-L, responsable de la différenciation et la maturation de la lignée ostéoclastique (33,34), puis de la libération du calcium nécessaire à la minéralisation du tissu osseux. En cas de déficience, le turn over osseux et augmenté, aboutissant à une perte à la fois du volume et de la densité osseuse. La matrice collagénique affaiblie, micro fissures, hypominéralisation, ostéopénie et ostéoporose surviennent fréquemment.
Une équipe chinoise a comparé l’aspect de fémurs d’adolescents selon leur taux sanguin de vitamine D (35). En cas de carence, la densité et la trabéculation sont moindres. (Fig. 4)
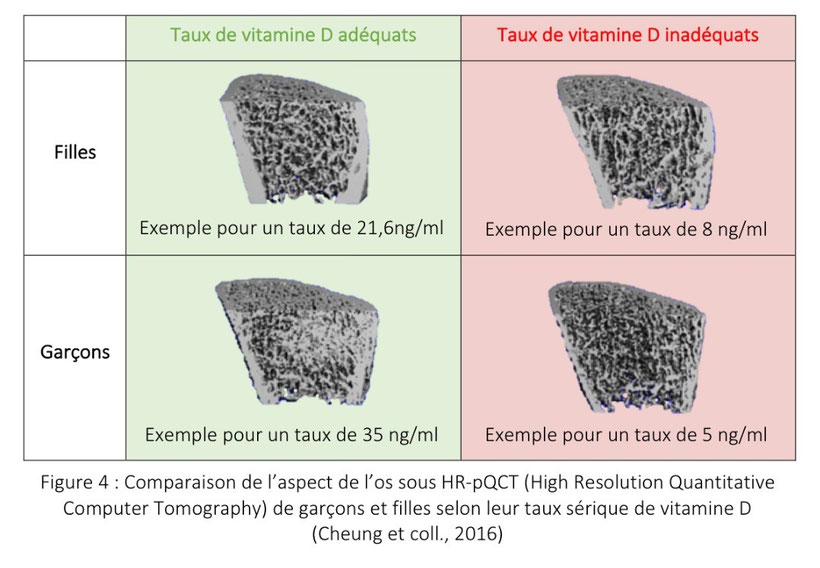
La vitamine D est donc essentielle à un métabolisme osseux performant et optimal. Les conséquences dentaires de ce lien vitamine D - os sont donc facilement imaginables.
Parodontologie
En plus de son effet osseux, l'effet anti-microbien de la vitamine D impacte la progression des maladies parodontales et le développement de bactéries parodonto-pathogènes comme Porphyromonas gingivalis. À des niveaux insuffisants, la vitamine D entraîne
- une augmentation de la profondeur de poche (36)
- risque de parodontopathies augmenté de 33%
- risque d’inflammation gingivale augmenté de 20% (37)
Plus la supplémentation serait importante, plus l’effet protecteur de la vitamine D serait visible.
Une dose journalière de 800 à 1000UI, soit largement au-dessus des doses recommandées, permettrait une nette amélioration des signes cliniques, ainsi qu’une meilleure cicatrisation lors des phases de maintenance des traitements parodontaux (38).
Implantologie
De nombreux chercheurs ont étudié les bienfaits de la vitamine D sur l’osteointégration, par des apports à la fois topiques et systémiques. Elles sont, pour le moment, la plupart sur des modèles animaux.
Un taux adéquat en vitamine D permettrait :
- une augmentation de la différenciation ostéoblastique et donc une réduction significative de la destruction osseuse (39) et de la perte osseuse marginale (40)
- une promotion de la formation osseuse, in vitro et in vivo et une meilleure ostéointégration (41)
- une diminution de la réaction inflammatoire suite à la pose des implants (42)
- une baisse des taux d’échecs implantaires précoces (3% contre 9) (43)
Concernant les greffes osseuses, les études sont encore peu nombreuses mais toutes en concluent, en cas de taux optimaux :
- une formation osseuse accélérée (44)
- une augmentation de leur taux de survie (45) avec des risques d’infections réduits
Maladie carieuse
Les cellules sécrétrices de l’émail sont en réalité des cellules cibles de la vitamine D. Le lien avec la minéralisation des tissus dentaire fait l’objet de nombreux articles. Une hypovitaminose D entraîne donc :
- une prévalence augmentée des caries dentaires
- des complications pulpaires plus fréquentes, avec une dentine moins perméable (46)
- une hausse de l’incidence carieuse de l’enfant en cas de déficience de la mère au cours de la grossesse (47)
- une baisse du risque de MIH (Hypominéralisation des molaires et incisives) (48)
En extrapolant, on pourrait également étendre le champ d’action de la vitamine D à la prévention des cancers oro-faciaux et à une diminution des conséquences dentaires consécutives aux chutes. De façon plus globale, la vitamine D influence l’ensemble de la sphère orale, que ce soit au niveau du parodonte ou de la dent en elle-même, et donc le taux de perte des dents. Elle devient un réel indicateur de « bonne santé », essentielle au bon fonctionnement du corps humain mais également de l’ensemble bucco-dentaire.
De plus, les résultats de cette étude nous incitent à considérer de façon sérieuse de problème de l’hypovitaminose D dans notre pratique quotidienne. L’objectif ici n’est pas seulement d’équilibrer le patient pour la chirurgie ou les soins mais de participer à une homéostasie plus constante au long cours. Il apparaît évident que le dosage de la vitamine D devient une nécessité dans le bilan préopératoire de nos patients en odontologie. L’ostéointégration d’un implant, la survie d’une greffe osseuse mais également, la stabilité de l’os ou d’un traitement parodontal va évidemment dépendre d’un maintien à long terme d’un taux sérique adéquat.
Bibliographie
1. Nowson CA, McGrath JJ, Ebeling PR & al. (2012) « Vitamin D and health in adults in Australia and New Zealand: a position statement ». Med J Aust; 196: 686-687
2. Glendenning P, Chew GTJ (2015). « Controversies and consensus regarding vitamin D deficiency in 2015: whom to test and whom to treat? ». Med J Aust; 202 (9): 470-471
3. Holick, M. F., MacLaughlin, J. A., & Doppelt, S. H. (1981). Regulation of cutaneous previtamin D3 photosynthesis in man: skin pigment is not an essential regulator. Science 211(4482), 590‐593.
TC. (2008) « Vitamin D deficiency: a worldwide problem with health consequences. » Am J Clin Nutr. Apr;87(4):1080S-6S.
5. Maier GS, Jakob P. (2013) « Vitamin D deficiency in orthopaedic patients: a single center analysis » Acta Orthop Belg. Oct;79(5):587-91.
6. Bertrais S. Preziosi P. & coll. (2004) « Sociodemographic and Geographic Correlates of Meeting Current Recommendations for Physical Activity in Middle-Aged French Adults : the Supplémentation en Vitamines et Minéraux Antioxydants (SUVIMAX) Study ». Am J Public Health. September; 94(9): 1560–1566.
7. Mart Kull & coll. (2009) « Seasonal variance of 25-(OH) vitamin D in the general population of Estonia, a Northern European country » BMC Public Health.; 9: 22.
8.Gröber U, Kisters K, Adamietz IA. « [Vitamin D in oncology: Update 2015] ». Med Monatsschr Pharm. 2015 Dec;38(12):512-6.
9. Ma Y, Johnson CS, Trump DL. « Mechanistic Insights of Vitamin D Anticancer Effects ». Vitam Horm.2016;100:395-431
10. Zhao Y, Chen C & coll. « Comparative efficacy of vitamin D status in reducing the risk of bladder cancer: A systematic review and network meta-analysis ». Nutrition.2015 Dec 19
11. Liu PT, Modlin RL & coll. «Toll-like receptor triggering of a vitamin D-mediated human antimicrobial response ». Science. 2006 Mar 24;311(5768):1770-
12. Holick, M. F. (2006). High prevalence of vitamin D inadequacy and implications for health. Mayo Clinic Proceedings, 81(3), 353‐373.
13. Saggese, G., Federico, G., Balestri, M., & Toniolo, A. (1989). Calcitriol inhibits the PHA-induced production of IL-2 and IFN-gamma and the proliferation of human peripheral blood leukocytes while enhancing the surface expression of HLA class II molecules, 5(12), 329‐35.
14. Hyppönen, E., Läärä, E., Reunanen, A., Järvelin, M. R., & Virtanen, S. M. (2001). Intake of vitamin D and risk of type 1 diabetes: a birth-cohort study. Lancet (London, England), 358(9292), 1500‐1503.
15. Shabahang, M., Buras, R. R., Davoodi, F., Schumaker, L. M., Nauta, R. J., Uskokovic, M. R., ... Evans, S. R. (1994). Growth inhibition of HT-29 human colon cancer cells by analogues of 1,25-dihydroxyvitamin D3. Cancer Research, 54(15), 4057‐4064.
16. Nagpal, S., Na, S., & Rathnachalam, R. (2005). Noncalcemic actions of vitamin D receptor ligands. Endocrine Reviews, 26(5), 662‐687.
17. Holick, M. F. (2006). Calcium plus vitamin D and the risk of colorectal cancer. The New England Journal of Medicine, 354(21), 2287‐2288; author reply 2287‐2288.
18. Chung, I., Han, G., Seshadri, M., Gillard, B. M., Yu, W., Foster, B. A., ... Johnson, C. S. (2009). Role of VDR in anti-proliferative effects of calcitriol in tumor-derived endothelial cells and tumor angiogenesis in vivo. Cancer research, 69(3), 967‐975.
19. Tangpricha, V., Spina, C., Yao, M., Chen, T. C., Wolfe, M. M., & Holick, M. F. (2005). Vitamin D deficiencyenhances the growth of MC-26 colon cancer xenografts in Balb/c mice. The Journal of Nutrition, 135(10), 2350‐2354.
20. Grant, W. B. (2002). An estimate of premature cancer mortality in the U.S. due to inadequate doses of solar ultraviolet-B radiation. Cancer, 94(6), 1867‐1875
21. Kilpinen-Loisa, P., Arvio, M., Ilvesmäki, V., & Mäkitie, O. (2009). Vitamin D status and optimal supplementation in institutionalized adults with intellectual disability. Journal of Intellectual Disability Research: JIDR, 53(12), 1014‐1023.
22. Yeshokumar, A. K., Saylor, D., Kornberg, M. D., & Mowry, E. M. (2015). Evidence for the Importance of Vitamin D Status in Neurologic Conditions. Current Treatment Options in Neurology, 17(12), 51.
23. Annweiler, C., Llewellyn, D. J., & Beauchet, O. (2013). Low serum vitamin D concentrations in Alzheimer’s disease: a systematic review and meta-analysis. Journal of Alzheimer’s Disease: JAD, 33(3), 659‐674.
24. Wang, L. & coll (2012). Circulating 25-hydroxy-vitamin D and risk of cardiovascular disease: a meta-analysis of prospective studies. Circulation. Cardiovascular Quality and Outcomes, 5(6), 819‐829.
25. Anderson, J. L. & coll. (2010). Relation of vitamin D deficiency to cardiovascular risk factors, disease status, and incident events in a general healthcare population. The American Journal of Cardiology, 106(7), 963‐968.
26. Li F & coll., (2011). Vitamin D deficiency is associated with decreased lung function in Chinese adults with asthma. Respiration; International Review of Thoracic Diseases, 81(6), 469‐475.
27. Black, P. N., & Scragg, R. (2005). Relationship between serum 25-hydroxyvitamin d and pulmonary function in the third national health and nutrition examination survey. Chest, 128(6), 3792‐3798.
28. Pittas A & coll. (2006). Vitamin D and calcium intake in relation to type 2 diabetes in women. Diabetes Care, 29(3), 650‐656.
29. Yavuz, B., Ertugrul, D. T., Cil, H., Ata, N., Akin, K. O., Yalcin, A. A., ... Tutal, E. (2009). Increased levels of 25 hydroxyvitamin D and 1,25-dihydroxyvitamin D after rosuvastatin treatment: a novel pleiotropic effect of statins? Cardiovascular Drugs and Therapy, 23(4), 295‐299.
30. Broe, K. E. & coll. (2007). A higher dose of vitamin d reduces the risk of falls in nursing home residents: a randomized, multiple-dose study. Journal of the American Geriatrics Society, 55(2), 234‐239.
31. Sohl, E. & coll. (2013). Vitamin D status is associated with functional limitations and functional decline in older individuals. The Journal of Clinical Endocrinology and Metabolism, 98(9), E1483‐1490.
32. Plotnikoff, G. A., & Quigley, J. M. (2003). Prevalence of severe hypovitaminosis D in patients with persistent, nonspecific musculoskeletal pain. Mayo Clinic Proceedings, 78(12), 1463‐1470.
33. Jimi E. et coll. (1996). Osteoclast function is activated by osteoblastic cells through a mechanism involving cell-to-cell contact. Endocrinology, 137(8), 2187‐2190.
34. Yasuda, H & coll.(1998). Osteoclast differentiation factor is a ligand for osteoprotegerin/osteoclastogenesis-inhibitory factor and is identical to TRANCE/RANKL. Proceedings of the National Academy of Sciences of the United States of America, 95(7), 3597‐3602
35. Cheung, T. F. & coll. (2016). Prevalence of vitamin D insufficiency among adolescents and its correlation with bone parameters using high-resolution peripheral quantitative computed tomography. Osteoporosis International
36. Zhan, Y. & coll. (2014). Prospective Study of Serum 25-hydroxy Vitamin D and Tooth Loss. Journal of Dental Research, 93(7), 639‐644.
37. Dietrich, T., Joshipura, K. J., Dawson-Hughes, B., & Bischoff-Ferrari, H. A. (2004). Association between serum concentrations of 25-hydroxyvitamin D3 and periodontal disease in the US population. The American Journal of Clinical Nutrition, 80(1), 108‐113.
38. Garcia, M. N. & coll. (2011). One-year effects of vitamin D and calcium supplementation on chronic periodontitis. Journal of Periodontology, 82(1), 25‐32.
39. Satué M. & coll. (2013). UV photoactivation of 7- dehydrocholesterol on titanium implants enhances osteoblast differentiation and decreases Rankl gene expression. Acta Biomaterialia, 9(3), 5759‐5770.
40. Salomó-Coll, O. & coll. (2015). Topical applications of vitamin D on implant surface for bone-to-implant contact enhance: a pilot study in dogs part II. Clinical Oral Implants Research.
41. Javed, F. & coll. (2016). Efficacy of Vitamin D3 Supplementation on Osseointegration of Implants. Implant Dentistry, 25(2), 281‐287.
42. Satué, M., Monjo, M., Ronold, H. J., Lyngstadaas, S. P., & Ramis, J. M. (2016). Titanium implants coated with UV-irradiated vitamin D precursor and vitamin E: in vivo performance and coating stability. Clinical Oral Implants Research.
43. Mangano et coll. (2016) « Is Low Serum Vitamin D Associated with Early Dental Implant Failure? A Retrospective Evaluation on 1625 Implants Placed in 822 Patients » Mediators of Inflammation
44. Hong, H.-H., Yen, T.-H., Hong, A., & Chou, T.-A. (2015). Association of vitamin D3 with alveolar bone regeneration in dogs. Journal of Cellular and Molecular Medicine, 19(6), 1208‐1217.
45. Cantorna, M. T., Hayes, C. E., & DeLuca, H. F. (1998). 1,25-Dihydroxycholecalciferol inhibits the progression of arthritis in murine models of human arthritis. The Journal of Nutrition, 128(1), 68‐72.
46. Souza AP.,Kobayashi TY.,Lourenço Neto N.,Silva SMB.,Machado MAAM.,& Oliveira TM.(2013). Dental manifestations of patient with vitamin D-resistant rickets. Journal of Applied Oral Science, 21(6), 601‐606.
47. Tanaka, K. & coll. (2015). Higher vitamin D intake during pregnancy is associated with reduced risk of dental caries in young Japanese children. Annals of Epidemiology, 25(8), 620‐625.
48. Kühnisch, J., Thiering, E., Kratzsch, J., Heinrich-Weltzien, R., Hickel, R., Heinrich, J., (2015). Elevated serum 25(OH)-vitamin D levels are negatively correlated with molar-incisor hypomineralization. Journal of Dental Research, 94(2), 381‐387.
Retour Aux articles Scintifiques