La parodontologie lasers assistée, une réalité scientifique incontestable #1
Dossier Laser, mode d'emploi
AO News #45 - Octobre 2021
Introduction
Il n’est nul besoin aujourd’hui de vouloir convaincre les réfractaires qui ne souhaitent pas voir progresser la Médecine dentaire ….
Chacun est libre de son choix, sous réserve de disposer des compétences nécessaires et des mises à jour de ses connaissances qui permettent de proposer aux patients TOUTES les options thérapeutiques disponibles.
Les résultats des recherches des nombreuses Universités Européennes confirment tous les effets bénéfiques des lasers médicaux correctement utilisés par des praticiens correctement formés. Il est temps de faire évoluer nos critères de bonne thérapeutique parodontale, et n’oublions pas que l’anesthésie a été longtemps délaissée au profit de l’arsenic …... que l’apport de mercure dans les tissus humains était accepté …. Sans oublier les vingt années de chemin de croix des pionniers de l’Implantologie …. Essayons juste d’éloigner l’intolérance des égos au seul profit de nos patients et du respect de notre mission prioritaire qui est de conserver le plus longtemps possible la sphère endo-buccale dans son état naturel. Les lasers peuvent-ils nous aider dans cette mission ? Essayons de répondre à cette question avec sincérité confraternelle !
25 années de recherches et de cautions scientifiques
Comment fonctionne le rayonnement laser ?
C’est en général un milieu actif placé dans une cavité résonnante qui va produire les photons du rayon laser par émission stimulée au cours de son excitation par un dispositif extérieur (Fig. 1) (Chavouin JP, Brunetaud JM et coll. 1995); A la sortie, les photons sont focalisés par une lentille vers la fibre optique de transmission et pris en charge par le spectre des ondes électromagnétiques, comme toutes les ondes visibles ou invisibles de notre univers terrestre.
Pour les lasers Diodes, le principe est la transformation de l’énergie électrique en énergie lumineuse dans de petites structures appelées Barrettes de Diodes. Ce sont ces 2 assemblements de matériaux différents qui provoquent le rayonnement lumineux par dopage des semi-conducteurs.
La lumière directionnelle et monochromatique des lasers médicaux (Classe 4) est en réalité une onde (Fig. 2) qui détermine la longueur d’onde de chaque laser (distance entre deux crêtes voisines).
Cette particularité permet au rayon laser d’être absorbé dans les tissus cibles en produisant de la chaleur (transformation de l’énergie vibratoire en énergie thermique) ou de traverser ces tissus en étant peu ou pas absorbés. Chaque tissu a une absorption différente en fonction de la longueur d’onde du rayonnement et les colorants présents modifie la distance de pénétration (Fig. 3) (Rey G, Missika P et coll. 2010).
Il y a donc deux familles de lasers médicaux très distinctes (Fig. 4) :
- les lasers absorbés sur quelques microns sans pénétration (lasers Er :YAG et CO2) ;
- les lasers pénétrants sur plusieurs centimètres qui ont peu d’action en surface mais peuvent provoquer des effets en profondeur (lasers Nd :YAG, Diodes, HeNe, Nd :YAP).

Fig. 1 Principe de production des rayonnements lasers

Fig. 3 Courbe d’absorption des différents lasers dans les principaux constituants cellulaires

Fig. 2 Une longueur d’onde est spécifique à chaque laser

Fig. 4 Schéma simplifié d’utilisation des lasers médicaux
Les effets des lasers médicaux
Les effets des lasers médicaux sont très simples et au nombre de quatre, il est donc inutile de chercher des complications dans le réglage de multiples protocoles thérapeutiques.
Ces effets sont : (Fig. 5) (Rey G. 2001 – 2010) (Dilouya D, Missika P et coll. 2019)
- effets ablatifs de volatilisation des tissus (qui sont des effets thermiques très forts) ;
- effets thermiques maitrisés (qui s’échelonnent entre la simple vasodilatation et la carbonisation) ;
- effets de décontamination par action bactéricide et virucide sur les pathogènes ;
- effets de biostimulation (photobiomodulation) qui accélèrent la synthèse de l’ATP et la mitose cellulaire en plus d’une action antalgique et anti-inflammatoire très efficace.
Note : avec les lasers pulsés de forte puissance de crête (Er :YAG, Nd :YAG, Nd :YAP) il existe également un effet de poussée dénommé effet canon très utile en endodontie et en chirurgie osseuse.
A chacun de ces effets lasers correspond une température d’échauffement des tissus cibles. La collaboration entre les industriels et notre équipe scientifique
concerne principalement la sécurité de l’utilisation des lasers médicaux en maitrisant avec précision les températures correspondant aux effets recherchés. Plus de 10 années ont été nécessaires
avant la mise au point des lasers « WISER » (fabriqués par Lambda et distribués en France par Kaelux) qui permettent (en mono ou en Tri longueur d’onde) de choisir directement l’effet souhaité
avec la sécurité d’obtenir la température la plus favorable à cet effet laser.
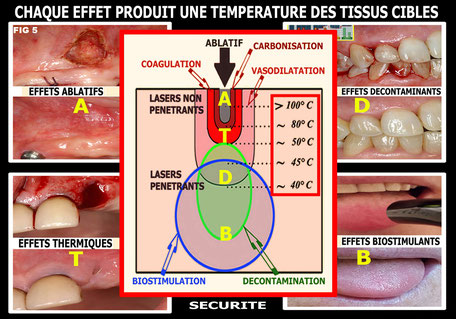
Fig. 5 Les 4 effets principaux des lasers et la température correspondante

Fig.6 Wiser 980 nm - Wiser Tri longueur d’onde
Le diamètre de la fibre optique de transmission est indiqué pour chaque effet, et plusieurs réglages sont possibles en fonction de la fragilité des tissus cibles, de la complexité anatomique éventuelle et de l’intensité de la pathologie diagnostiquée. En décontamination parodontale, 4 réglages (faibles, moyens, forts ou très forts) sont directement disponibles sur l’écran, et le choix dépend de l’étude des tissus cibles irradiés, ainsi que du type et de la quantité de bactéries décelées dans l’examen bactériologique (Fig.7) (Mouton C, Robert JC. 1994)
Recherches et actualité médicale
Toutes les recherches effectuées ont été réalisées en parfaite indépendance scientifique, par des laboratoires n’ayant aucune contrainte industrielle ou commerciale. Les premières études in vitro sur l’effet bactéricide des lasers datent de la fin des années 90 et du début des années 2000 (Biomatech - Pasteur - Fournier) (Fig. 8 et 9) (Rey G. 2001).
Elles ont conclu à l’inefficacité du rayonnement laser utilisé seul et à une efficacité très faible du Peroxyde d’Hydrogène à 3 %. Par contre, ces études ont démontré un effet bactéricide réel du rayonnement laser utilisé sous peroxyde d’hydrogène à 3 % sur l’ensemble des pathogènes parodontaux et particulièrement sur le complexe rouge de Socransky (Socransky SS, Haffajee AD. 1998).
Ces résultats ont été publiés dès le 3ème trimestre 2000 pour les traitements parodontaux et dès 2001 pour le traitement des péri-implantites. (Fig.10 D) Ils ont été confirmés par les études italiennes à l’Université de Milan Bicocca et publiés en 2007 par le Professeur Gianluigi Caccianiga.
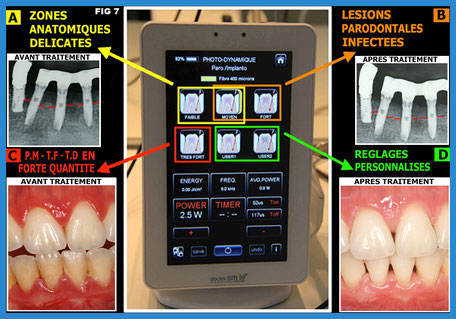
Fig. 7 Avec chaque effet, le praticien a le choix des réglages faibles, moyens ou forts

Fig. 9 Deuxième étude Laboratoire Fournier

Fig. 8 Première étude Biomatech/Pasteur

Fig. 10 Conclusions des études en laboratoires in vitro
Entre 2005 et 2015, de nombreuses études in vivo et in vitro ont été menées en Europe. Elles ont toutes confirmé l’efficacité du protocole parodontal décontaminant mis au point à Montpellier entre 1995 et 2000 (Rey G, Missika P. 2010-2013) (Caccianiga G, Rey G et coll. 2016). Entre 2017 et 2021, une collaboration est demandée par les services d’Infectiologie des CHU dans le cadre d’une recherche sur les bactéries antibio-résistantes, telles que Staphylococcus Aureus.
De nouvelles études in vivo et in vitro sont réalisées en 2018, 2019 et 2020 en collaboration entre l’I.N.T.I., (partenaire de l’Université de Montpellier), le Centre Hospitalier d’Annecy et les CHU de Paris Ouest, Garches, Nantes et Lyon (Fig. 11 et 12).
Les bons résultats obtenus avec le protocole décontaminant (laser sous H2O2 10 vol.) ont été actés par les laboratoires (Fig. 11) et ont permis des études in vivo à l’Ecole Nationale Vétérinaire d’Alfort (ENVA). (Rey G, Bonnin P, Bland S. 2018)

Fig. 11 Etude sur Staphylococcus Aureus en 2018.

Fig. 12 Etudes in Vivo à l’E.N.V.A. en 2019
Par la suite, des cas cliniques d’infections résistantes aux antibiotiques sont traités avec succès dans différentes cliniques (Fig. 13) et le traitement d’une ostéonécrose antibiorésistante permettra de montrer également une action bactéricide (Fig. 14) sur : Raoultella Ornithinolytica, Proteus Mirabilis, Enterococcus Faecalis.

Fig. 13 Efficacité du protocole sur les bactéries antibiorésistantes

Fig. 14 Traitement d’une infection osseuse et résultat bactériologique négatif
Protocole général de traitement des parodontites infectieuses
Nous ne pouvons détailler ici l’importance du diagnostic initial et de la mise en place d’un plan de traitement cohérent, qui fait l’objet d’un long chapitre dans le dernier ouvrage Traitements Parodontaux et Péri-implantaires lasers Assistés. (Rey G. 2021)
Nous rappelons aux confrères que cette première consultation parodontale est indispensable et qu’il est nécessaire de prévoir un temps suffisant pour réaliser tous les examens utiles et donner au patient les informations essentielles, particulièrement pour la maitrise de l’hygiène bucco-dentaire spécifique à chacun.
Ne pas le faire est un refus de notre responsabilité médicale sur la santé générale de nos patients… et aussi d’accepter de pratiquer un acte chirurgical éventuel, sans vérifier que la flore présente est compatible avec la chirurgie envisagée (ce qui semble en contradiction avec les règles élémentaires de tout acte chirurgical ….).
Note : Il est évident qu’une étude bactériologique est souhaitable et que la présence d’un microscope à contraste de phase est nécessaire dans un cabinet pratiquant la Parodontologie. (Van Winkelhoff AJ et coll. 2005) (Megle J, Chapple I. 2015)
D’autre part, l’information donnée au patient sur son état de santé antérieur ne sera pas complète pour obtenir un consentement éclairé. Peut-être une double faute évitable ?
Le matériel utile
Le matériel strictement nécessaire est très simple :
- un détartreur dentaire ultrasonique, type EMS Air Flow Prophylaxis Master ou Airflow Master Piezon ;
- un aeropolisseur efficace (il existe déjà sur les appareils EMS cités) ;
- un laser au rayonnement pénétrant (un simple laser Diode bien réglé est parfait en Parodontologie), tels que les Wiser 980 nm et Wiser Tri ondes ;
- des aides optiques de grossissement 2,5 à 3,5.
La préparation parodontale avant utilisation du laser (Rey G, Missika P. 2010)
Elle est réalisée sans lambeau d’accès mais sous anesthésie locale. Les interventions s’effectuent en général par hémi arcade, avec un délai d’attente suffisant entre deux traitements pour permettre au patient une bonne maitrise de l’arcade précédemment traitée).
4 actes successifs sont réalisés.
1. Débridement gingival ultrasonique jusqu’au contact osseux en respectant un mouvement tangentiel au cément radiculaire (sous irrigation de povidone iodée diluée à 10 %) (Fig. 15.1)
2. Détartrage rigoureux sous eau décontaminée (le débridement préalable donne une meilleure vision sous gingivale). Cette inversion détartrage / débridement permet également un excellent rinçage de la bétadine présente dans les tubulures de l’ultrason, sans perte de temps (Fig. 15.2)
3. Un aéropolissage minutieux des racines accessibles pour rouvrir les tubulis dentinaires obturés par la smear layer et éliminer les résidus tartriques (Fig. 15.3)
4. Après rinçage complet au spray, l’ensemble des poches parodontales est oxygéné par dépôt d’eau oxygénée à 10 vol au plus profond des lésions accessibles sans noyer la bouche d’eau oxygénée, l’assistante aspirant ce qui est en superflu. Seule la partie gingivale débridée est remplie pour oxygéner les tissus parodontaux infectés.
Cette action est également possible avec les monodoses Sioxyl (peroxyde d’hydrogène + Glycerophosphate de sodium) mises au point par Gianluigi Caccianiga (Fig.15.4)
Le peroxyde d’hydrogène ou le Sioxyl sont laissés environ 3 minutes avant d’activer la fibre laser dans la lésion oxygénée. (Fig.15.4)
La décontamination laser assistée (Bezzina, Moulierac, Rocca. 2010) (Andersen R, Loebel N et coll. 2007)
Quel laser faut-il utiliser ?
- Il est indispensable d’irradier les tissus préalablement oxygénés avec un rayonnement pénétrant pour espérer une bonne décontamination de l’ensemble des tissus infectés en profondeur. (Rey G, Caccianiga G. 2010-2017)
Les lasers non pénétrants (Er :YAG, CO2) n’ont aucune action décontaminante réelle mais leur utilisation peut être une option intéressante pour volatiliser des tissus nécrotiques et obtenir une anatomie gingivale favorable à une cicatrisation plus rapide.
- Les lasers Nd :YAG et Nd :YAP sont pénétrants (surtout le Nd :YAG), mais très thermiques (surtout le Nd :YAP !). Leur utilisation en parodontologie demande de l’expérience et beaucoup de prudence avec des rafales courtes et des temps de repos longs.
- De nombreux lasers Diodes sont réglés avec une action thermique forte qui coagule les protéines et détruit les tissus vivants, ce qui n’est pas souhaitable en parodontie.
Ils peuvent occasionner des brulures en profondeur et leur utilisation nécessite des précautions pour limiter les effets thermiques non souhaitables.
Les réglages efficaces possibles avec les lasers Diodes
Le réglage moyen souhaitable est une puissance de crête d’environ 2,5 w pour maintenir une bonne pénétration, mais avec un rapport d’environ 30 % de temps de pulse (Ton) et 70 % de temps de repos (Toff).
La puissance moyenne obtenue est d’environ 0,8 W et la fréquence doit être égale ou supérieure à 6000 Hz (6000 impacts par seconde) pour que le cycle décontaminant dioxygène - oxygène singulet - oxygène triplet soit le plus efficace possible (Rey G, Missika P, Caccianiga G. 2010-2016-2019).
Deux lasers Diodes ont été mis au point suivant ces principes par l’industrie italienne Lambda :
- le laser Wiser 980 nm, très sécurisant et très facile à utiliser sans risque de brulure interne involontaire ;
- le laser Wiser Tri (810 nm + 635 nm + 450 nm) qui est réglé avec 40 % de Ton pour une meilleure action sur les bactéries très résistantes (S.A., P.M., E.F., T.F., …). Avec ce laser, notre conseil en parodontologie classique est de régler un Ton à 20 % et un Toff à 80 % afin de réduire la puissance moyenne à 0,8 w.
Ainsi, l’extrémité de la fibre (au contact du sang) carbonise moins facilement et permet une pénétration maximum du rayon laser. Il est, malgré tout, toujours préférable de nettoyer son extrémité avec une compresse désinfectante lorsque cela est nécessaire.
L’action de décontamination
L’action de la fibre se fait verticalement de haut en bas jusqu’au contact osseux pour pénétrer au maximum (Fig. 16.1). Le déplacement latéral autour des dents est effectué au fur et à mesure pour irradier l’ensemble des tissus infectés (gingivaux, osseux et dentaires) dans les lésions vestibulaires, proximales ou intrabuccales (Fig. 16.2).
Résultat postopératoire immédiat
L’effet de vasodilatation qui accompagne la décontamination (et conjointement la biostimulation) permet l’apport de cellules sanguines dans les lésions parodontales (Fig. 16.3) (Rey G. 2010-2018)
Le sang oxygéné est laissé en place sans aucun rinçage. Nous essuyons simplement les dents et l’excès de sang avec une compresse en indiquant au patient de laisser au maximum les petits caillots sanguins protecteurs postopératoires (Fig. 16.4).

Fig.15 Les 4 étapes préparatoires avant la décontamination lasers assistée

Fig. 16 Les 4 étapes de l’action décontaminante laser assistée
Les résultats cliniques et radiographiques
Tous les traitements réalisés ont fait l’objet de 6 séances au total :
- 1 consultation initiale complète avec toutes les informations nécessaires ;
- 4 traitements par hémi arcade à environ 1 mois d’intervalle ;
- 1 séance de cicatrisation : vérification générale, conseils, maintenance et programme général à prévoir pour le patient ;
- aucun des cas présentés n’a reçu une antibiothérapie en complément du traitement laser.
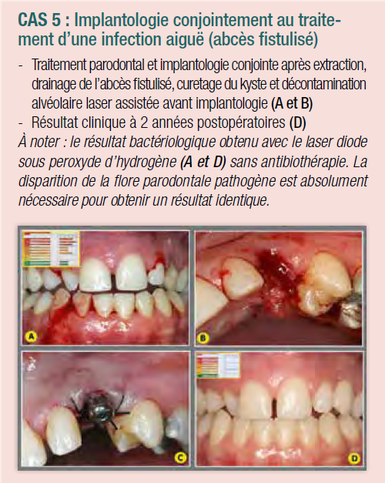
Chaque cas ayant été réalisé de manière identique, il est donc suffisant de montrer les résultats obtenus cliniquement et radiographiquement pour que le lecteur puisse juger de l’efficacité de ce type de traitement.






Hygiène buccodentaire et maintenances
Toutes les recherches in vitro et in vivo ont démontré l’efficacité du protocole laser assisté pour éradiquer les bactéries parodonto-pathogènes de l’environnement parodontal, mais comme toute maladie infectieuse, celle-ci peut récidiver si les facteurs aggravants ne sont pas maitrisés.
L’hygiène quotidienne buccodentaire
L’absence d’hygiéniste en France est imputable à nos élus et à nos représentants professionnels. C’est une anomalie lourde de conséquences pour notre exercice libéral et pour nos patients !! Le temps nécessaire à la motivation et à la surveillance jusqu’à la maitrise parfaite de l’hygiène buccodentaire est pénalisant pour les praticiens qui le font avec un maximum de conscience professionnelle et doivent donc recevoir la rémunération du temps passé ….
Nous avons résolu une partie de ce handicap en imprimant un petit fascicule général qui est remis à chaque patient à la consultation initiale avec les conseils spécifiques à son cas particulier. Les points essentiels sont le choix du matériel adapté, brosse électrique à mouvement vertical et hydropulseur, ainsi que les conseils d’utilisation (17,18,19). Tout ceci a fait l’objet de nombreux tests Franco-Italiens qui sont expliqués longuement dans nos formations universitaires.
Note : les mauvaises habitudes des patients sont parfois longues à modifier. C’est la raison de notre choix d’un traitement par hémi arcade qui nous donne avec la première et la dernière séance 6 rendez-vous d’une heure (parfois plus …) au cours desquels nous devons prendre le temps nécessaire pour améliorer la maintenance quotidienne laissée sous la responsabilité de nos patients.
Les maintenances en cabinet de soins (rôle futur des hygiénistes ?)
Elles sont prévues en moyenne une fois par an lorsque le patient maitrise les soins quotidiens. Après un traitement décontaminant, il est logique d’avoir une disparition de l’inflammation et donc une rétraction du niveau gingival qui va venir se placer physiologiquement par rapport au niveau osseux résiduel (Fig. 20 A et B).
Si l’hygiène buccodentaire (Fig.20 D) et les maintenances sont correctement effectuées, la cicatrisation gingivale sera visible au bout de quelques mois (Fig.20 C). Elle annonce la bonne cicatrisation osseuse que nous vérifierons par simple radiographie panoramique de contrôle.
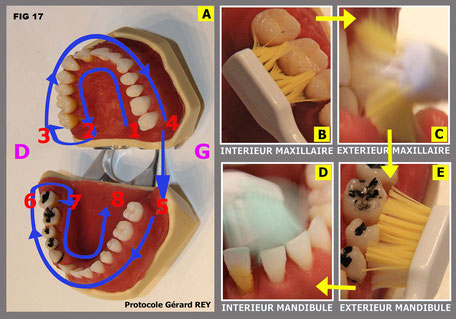
Fig. 17 L’enseignement de l’H.B.D. nécessite temps et explication

Fig. 19 Protocole utilisé depuis 20 années avec une efficacité vérifiée

Fig. 18 L’hydropulseur est seul capable d’assainir les poches parodontales profondes
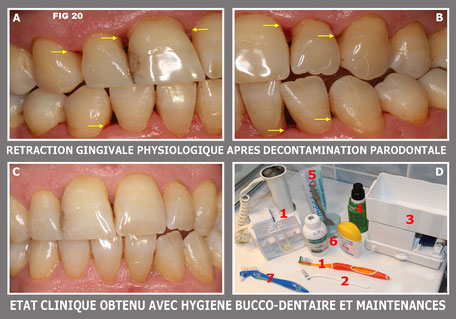
Fig. 20 La disparition des bactéries pathogènes et la maitrise de l’H.B.D. permettent une cicatrisation gingivale esthétique et protectrice
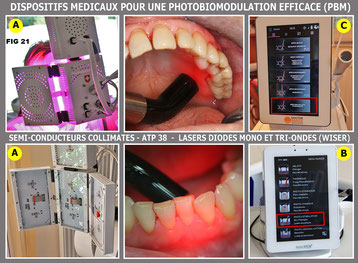
Fig. 27 L’intérêt de la PBM pour de bonnes suites opératoires et pour une excellente cicatrisation
A chaque maintenance, il est possible et vivement conseillé d’effectuer une photobiomodulation (PBM) avec un rayonnement pénétrant, (Ozcelik O, Cenk Haytac M et coll. 2008), type laser Diode ou LED (Light Emitting Diode) comme l’ATP 38 dont l’utilité rend de grands services dans de nombreux domaines médicaux et chirurgicaux.
- Utilisation des lasers Diodes en PBM. (Caccianiga G, Baldoni M et coll. 2016)
Cela s’est réalisé avec les lentilles courbes défocalisantes pour l’intérieur de la cavité buccodentaire, ou avec la pièce à main Flap Top, plus spécifique pour une irradiation externe ou vestibulaire antérieure.
Les réglages et les conseils d’utilisation sont directement indiqués sur les écrans des lasers Wiser® (980 nm et Tri Ondes) (Fig. 21 B et C).
- La PBM. et les 7 longueurs d’onde de l’ATP 38
Pour la cavité buccodentaire, elle se fera par voie externe en enveloppant les maxillaires avec 3 volets (Fig. 21 A). Le programme de 12 minutes (antalgique, anti-inflammatoire, biostimulation) est bien adapté en postopératoire, et par la suite, un programme plus court de biostimulation favorise l’oxygénation cellulaire, la circulation sanguine et l’activité des fibroblastes. (Rey G. 2018).
Conclusions … et prévention !
Cette petite parution a juste la prétention d’une information confraternelle sincère sur notre expérience de l’utilisation des lasers médicaux dans le traitement des infections parodontales et péri-implantaires … une expérience de plus de 25 années, vérifiée par des centaines de praticiens utilisateurs, et des milliers de patients satisfaits !
Quand cette expérience clinique est confirmée par plusieurs équipes universitaires et de nombreux tests laboratoires … cela mérite peut-être un intérêt professionnel des confrères qui souhaitent évoluer, simplifier leur exercice en restant efficaces, et diminuer sérieusement les prescriptions antibiotiques.
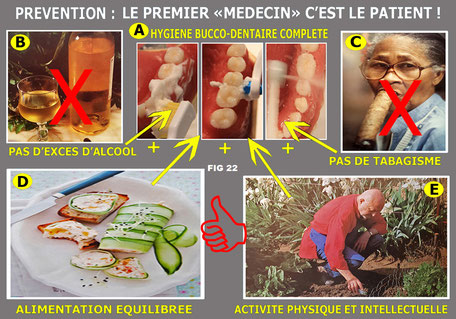
Fig. 28 Une bonne image vaut mieux qu’un long discours !
Vous trouverez l’ensemble de ces recherches, de ces traitements et des protocoles parodontaux utilisables en omnipratique dans le dernier ouvrage paru en 2021 et dont plusieurs versions (anglaise, italienne, roumaine) seront disponibles prochainement. Ouvrage vendu pour financer nos recherches médicales

Bibliographie
Andersen R, Loebel N, Hammond D, Wilson M. Treatment Of Periodontal Diseases By Photodisinfection Compared To Scaling And Root Planning. J Clin Dent. 2007 ; 18:34-8
Avril Jl, Dabernat H, Denis F, Monteil H. « Bactériologie Clinique » Ed Ellipse 2000
Bezzina-oulierac Me, Rocca Jp. Laser Et Parodontie En Parodontie Médicale. Innovations Cliniques, 2nd Ed. Edcdp, 2010, 431-447
Caccianiga G, Cambini A, Donzelli E, Baldoni M, Rey G, Paiusco A. Effects Of Laser Biostimulation On The Epithelial Tissue For Keratinized Layer Differentiation. Journal Of Biological Regulators And Homestatic Agents. 2016 ; Vol 30 N°2 : 99-105
Caccianiga G, Baldoni M Et Coll. « Effects Of Laser Biostimulation On The Epithelial Tissue For Keratinized Layer Differenciation” Journal Of Biological Regulators And Hemostatic Agents 2016 ; Vol.30 N°2 : 99-105
