Nécessité de combler ou pas après une extraction
Indications, description des protocoles (pré-implantaires ou pas), matériaux en fonction des indications
Le dossier AO News : l'alvéole, c'est essentiel
AO News #60 - Septembre 2023
Introduction
Un comblement alvéolaire fait suite à une avulsion et l’on doit considérer la gestion du site extractionnel comme point clé de la préservation des tissus durs et mous.
Une extraction dentaire a 2 conséquences biologiques : résorption et perte de qualité tissulaires. Elles induisent la prise en compte du degré de celles-ci selon sa destination de remplacement dentaire.
Les causes de l’avéolyse sont :
- l’arrêt du potentiel de stimulation bio électrique de la dent.
- la migration rapide de l’épithélium bloquant la croissance osseuse.
- l’exposition de l’os qui entraîne une ostéoclasie réactionnelle.
Atwood et Schroop (1,2) ont décrit la résorption conséquence directe de l’avulsion.
L’évolution dimensionnelle de l’alvéole après l’avulsion génère :
- une perte de 20 % à 4 semaines
- une perte de 60 à 80 % dans les 2 ans
Elle est augmentée par le port de prothèse amovible sur le site extrait et cette donnée doit être largement envisagée, porteuse d’effets négatifs parfois irréversibles si elle insuffisamment gérée.
Elle est associée à la dépréciation quantitative comme qualitative de la gencive.

Une classification de l’anatomie de l’alvéole après extraction a été proposée par Elian, Cho, Smith et Tarnow (3) (Fig. 1)
Elle permet de préciser en quoi l’anatomie influence le plan de traitement et le choix des reconstructions.
Il existe 3 sources d’apport sanguin à la table osseuse externe.
- Le ligament parodontal : majoritairement perdu avec l’avulsion.
- Le périoste : conservé si intervention en mode flapless.
- L'os spongieux : selon Mariano Sanz, l’épaisseur de la table externe est inférieure à 1mm dans 95 % des cas ce qui réduit largement la présence spongieuse (4).
Un point clé lors d’une extraction est de penser à la préservation de la table osseuse externe.
D’après Fickl, l’élévation d’un lambeau de pleine épaisseur entraîne toujours une ostéoclasie réactionnelle de l’os mis à nu (5).
La réflexion biologique comme temporelle dans les actes est essentielle avant la mise en œuvre des moyens : greffon, biomatériau, produits dérivés du sang et membrane utilisés ont vocation à revascularisation et maintien.
Les capacités ostéo-conductrices, ostéo-inductrices ou initiatrices des biomatériaux ou produits autologues ont été en effet largement décrits.

Plus largement, la qualité résiduelle des murs alvéolaires après extraction et notamment la présence qualitative de la table externe porteuse de cellules de la lignée hématopoïétique mais souvent exclusivement corticalisée, la dimension du « gap » entre la face externe de l’implant et la paroi vestibulaire interne de l’alvéole (si destination implantaire immédiate), vont fonder la valeur tissulaire cicatricielle. (Fig. 2)
Ces paramètres vont prévaloir à la destination implantaire immédiate ou reportée où à la logique d’inter de bridge après cicatrisation ou reconstruction.
En dehors de l’indication, deux techniques existent pour anticiper ces risques.
- La technique de Langer avant extraction qui consiste à mettre en condition les tissus péri-dentaires avant celle-ci. Elle permet, par la réalisation de gestes progressifs avant le jour de l’extraction, d’obtenir la fermeture naturelle du lambeau sans tension en meulant progressivement la couronne de la dent à extraire jusqu’à son recouvrement total.
Cette approche, facilement réalisable, impose toutefois une multiplication de rendez-vous et la disponibilité des parties. Son pronostic est favorable et reproductible (6).
- La réalisation d’un greffon épithélio-conjonctif prélevé au palais lors de l’extraction, outre l’éventuel comblement. Cette approche nécessite une fermeture étanche du greffon entourant les berges de l’alvéole.
L’objectif global est la conservation et la reformation tissulaire du volume alvéolaire maximal afin d’assurer les contours et la qualité muqueuse pour un environnement péri-implantaire ou un inter de bridge ad hoc en terme fonctionnel, de confort et d’esthétique.
La fermeture des berges dans ces deux approches a pour objectif le maintien du caillot dans un milieu fermé propice à cette reformation tissulaire la plus favorable.
Destination implantaire
Les questions qui se posent dans le cadre d’une avulsion à cette destination sont celles-ci :
- l’anatomie affecte-t-elle le plan de traitement ?
- quelle est l’importance de l’espace alvéole/implant ?
- un implant immédiat permet-il de conserver la table vestibulaire ?
Quelle est alors l’utilité de systématiquement combler l’alvéole qui nécessitera de protéger le matériau d’une invagination tissulaire notamment en cas d’implant immédiat ?
Si le gap entre la corticale interne et l’implant est inférieur à 1, 5mm, la fermeture d’un éventuel lambeau au jour de l’extraction impliquera un décalage de la ligne de jonction muco-gingivale vers la crête avec une perte de vestibule et d’harmonie.
On évitera alors d’effectuer un lambeau en laissant l’alvéole cicatriser par 2ème intention.
Dans ce cas, et sur une anatomie post-extractionnelle de type1, la table vestibulaire ne subit pas de résorption réactionnelle et il va se produire :
- un envahissement alvéolaire par le caillot sanguin immédiat;
- la transformation du tissu de granulation en tissu conjonctif en 3 semaines en provenance du fond osseux alvéolaire et des résidus de ligament;
- la migration de l’épithélium des parois en 3 semaines;
- la calcification du tissu conjonctif en 4 à 6 semaines. L’alvéole sera alors remplie aux deux tiers par du tissu ostéoïde.
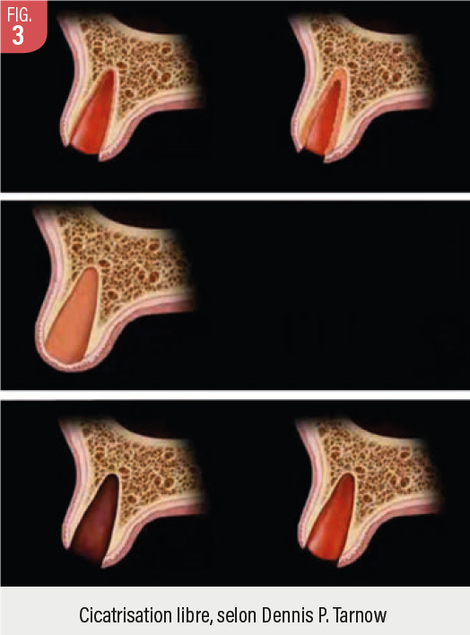
L’épithélium et le tissu conjonctif au bord de l’alvéole ne pouvant pas traverser de l’autre côté de l’alvéole tant que le tissu de granulation n’est pas arrivé en provenance des murs osseux, l’épithélium aura besoin du tissu conjonctif alvéolaire qu’il attend car il ne peut croitre au-delà du caillot qui n’est pas un apport sanguin immédiat.
(fig 3)
L’apport sanguin interne proviendra donc des murs osseux s’il existe assez d’os spongieux avec mise en place d’une compresse de cristallisation du caillot intra alvéolaire ou apport de matériaux en particules allogènes dans le gap en cas d’implant immédiat.
Il ne faut donc pas élever un lambeau pour avulser une dent et de ce fait ne pas tirer ce lambeau au-dessus du défaut. En effet, l’os viendra alors en premier puisque l’épithélium et le tissu conjonctif en provenance de l’alvéole sont freinés tant que l’alvéole n’est pas rempli de vaisseaux sanguins en provenance de l’os. Une absence de comblement est alors le meilleur choix.
Dennis Tarnow notamment pense que l’espace n’a que peu d’importance et que la fermeture du lambeau si les tables osseuses sont présentes n’est pas nécessaire même si le gap entre la corticale externe et l’implant est supérieur à 1,5 mm (7).
Avec une anatomie post-extractionnelle de type 2, alors il y aura formation d’un film de tissu conjonctif dans celui-ci laissé libre.
Si un lambeau est réalisé, le risque est que le tissu conjonctif du lambeau de fermeture migre dans l’espace puisque le lambeau est un pédicule avec son propre apport sanguin.
Le tissu conjonctif du lambeau migrera ainsi à l’intérieur du caillot plus vite que le jeune os en provenance de la table osseuse et du fond de l’alvéole.
En dehors d’une préparation anticipée comme exposée ci-dessus par étapes, l’alvéole sera dans ce cas comblée avec un biomatériau allogénique particulé à résorbabilité peu rapide afin de laisser la vascularisation diffuser aisément.
Nous privilégions :
- un comblement modestement compressif de type Bio-oss® (Geistlich),
- une compression progressive de plusieurs membranes de PRF comme apport de facteurs de croissance suturée de manière lâche sur la plaie alvéolaire avec une action prépondérante dans les premiers temps de stimulation des cellules ostéoprogénitrices comme décrit par Omar et Thomsen (8).
L’alvéole sera fermée :
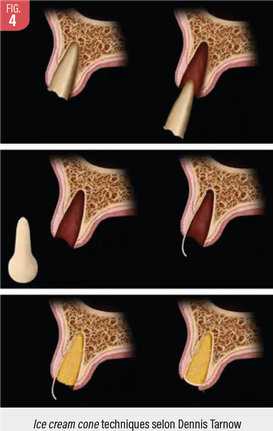
- soit par une technique ice cream cone (Dennis Tarnow) avec une membrane résorbable repliée sur la plaie alvéolaire. Nous utilisons la membrane Osseo Guard ®(ZimVie) (Fig. 4) ;
- soit par un greffon circulaire épithélio-conjonctif prélevé au palais et suturé pour garantir l’étanchéité de la plaie alvéolaire
En cas de compression par des membranes PRF, la fermeture se fera naturellement ou comme décrite ci-dessus selon le volume et la capacité de maintien des produits dans l’alvéole.
Il faut par ailleurs rappeler que la pose d’un implant immédiat ne préserve pas de la résorption de la table osseuse vestibulaire comme l’ont décrit Araujo et Lindhe (9, 10). L‘indication de l‘implantologie immédiate (post-extractionnelle) est assez limitée et n’est pas l’objet de l’avis ici proposé.
En cas d’anatomie alvéolaire de type 3 avec maintien des murs impossible après extraction, une protection a minima avant réévaluation doit être envisagée en sachant que tant l’apport sanguin que le maintien d’un apport tissulaire sont alors compromis à ce stade. C’est la situation clinique qui, au plus clair des choses, guidera le praticien.
Un comblement au sens sémantique du terme ne pourra être stabilisé. Le site étant dans ce cas souvent infecté, toute reconstruction y est prématurée.
Nous pratiquons alors un recouvrement de la plaie avec un sticky bone , évolution de la technique des concentrés plaquettaire type PRF décrite dès 2001 par Joseph Choukroun. Cette technique permet de capter plus de monocytes dans le PRF, afin de le rendre vers une transformation plus rapide des monocytes en macrophages afin d’augmenter l’effet de stimulation osseuse. (11, 12).
L’extraction dentaire à destination de pontic de bridge appellera une approche nuancée.
C’est bien la recherche d’un contour évitant une rétention alimentaire cervicale ou un contour esthétique anatomique favorable qui guideront le choix technique. Le futur pontic devra s’insérer sans contrainte de pression dans la partie crestale résiduelle. L’os n’aura pas vocation à être fonctionnel.
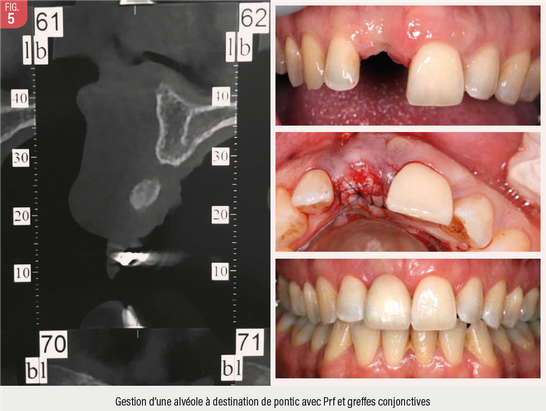
Dans l’absolu, les deux objectifs sont proches et la démarche clinique similaire en particulier dans les secteurs esthétiques. (Fig. 5)
Le dessin et le contrôle de l’éventuelle prothèse amovible seront essentiels dans le maintien tissulaire en attente de réalisation de la prothèse d’usage.
Conclusion
La question clé de l’utilisation ou non de biomatériaux ou de PRF réside dans l’indication post extractionnelle et leur mise en œuvre technique comme temporelle.
Au pur plan du travail au fauteuil, Il faut tenir compte des impératifs souvent évacués dans les articles mais ô combien fondamentaux dans la clinique du quotidien.
Le nombre de gestes, le pronostic garanti, l’aspect économique, la participation (selon la formule bien établie) directe et induite du patient au succès qu’il aura parfois du mal à pleinement appréhender dans ses contraintes jusqu’au résultat final.
Le maintien du volume extérieur et des contours naturels avec une gencive vascularisée et kératinisée doit être le point clé de l’objectif.
Bibliographie
1 Atwood DA, Willard AC. Clinical, cephalometric, and densitometric study of reduction of residual ridges. J Prosthet Dent1971; 26: 280–295
2. Schropp L, Wenzel A, Kostopoulos L, et al. Bone healing and soft tissue contour changes following single-tooth extraction: a clinical and radiographic 12-month prospective study. Int J Periodontics Restorative Dent 2003; 23: 313–323
3. Elian N, Cho SC, Smith E, Tarnow D. A simplified socket classification and repair technique”Pract Proced Aesthet Dent 2007;19(2) : 99-104
4. Fabio Vignoletti Paula Mariano Sanz Daniel Rodrigo Elena Figuero Conchita Martin Mariano Sanz Surgical protocols for ridge preservation after tooth extraction. A systematic review, Clin Oral Implant research Déc. 016
5. Stefan Fickl, Otto Zuhr, Hannes Wachtel, Wolfgang Bolz, Markus Huerzeler, Tissue alterations after tooth extraction with and without surgical trauma: a volumetric study in the beagle dog. J Clin Periodontology 2008 Apr;35(4):356-63.
6. Langer B. Soft tissus complications The esthetic dilemma Int J Maxillofac. Implant 2003 set oct ;18 (5) :767-8
7. Dennis Tarnow, The Single-Tooth Implant: A Minimally Invasive Approach for Anterior and Posterior Extraction Sockets, octobre 2019
8. Omar &Thomsen, Biomaterials 2012, Kawazoe T. Cell Transplant. 2012
9. Araújo MG, Sukekava F, Wennström JL, et al. Ridge alterations following implant placement in fresh extraction sockets: an experimental study in the dog. J Clin Periodontol 2005; 32: 645–652
10. Araújo MG, Lindhe J. Dimensional ridge alterations following tooth extraction. An experimental study in the dog. J Clin Periodontol 2005; 32: 212–218
11. Choukroun, J.; Adda, F.; Schoeffler, C.; Vervelle, A. Une opportunité en paro-implantologie: Le PRF. Implantodontie 2001, 42, 62.
12 Ghanaati, S.; Booms, P.; Orlowska, A.; Kubesch, A.; Lorenz, J.; Rutkowski, J.; Landes, C.; Sader, R.; Kirkpatrick, C.; Choukroun, J. Advanced platelet-rich fibrin: A new concept for cell-based tissue engineering by means of inflammatory cells. J. Oral Implantol. 2014, 40, 679–689.
