Nouvelles recommandations pour le traitementde la parodontite et de la péri-implantite : que doit savoir l’omnipraticien ?
Conférencier : Panos Papanou Responsable scientifique de séance : Julie Lamure

ADF 2023 morceaux choisis par la Team AO News - AO News #64 - Février 2024
La parodontite est une maladie inflammatoire chronique multifactorielle associée à des biofilms dysbiotiques et caractérisée par une destruction progressive du système d’attache. Ses principales caractéristiques comprennent la perte du support tissulaire parodontal, qui se manifeste par une perte d'attache clinique (CAL) et une perte osseuse alvéolaire évaluée radiographiquement, la présence de poches parodontales et de saignements gingivaux.
Le diagnostic de parodontite se fait sur le niveau d’attache clinique relevé au sondage. Ce dernier ne peut pas être attribué à une récession gingivale induite par un traumatisme, à des lésions carieuses dans la région cervicale, à des lésions endodontiques se drainant à travers le parodonte ou à une fracture dentaire.
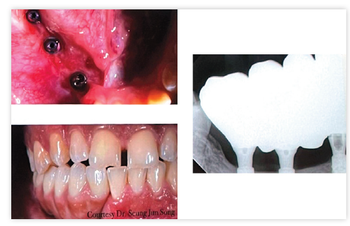
Pourquoi ne pas de baser sur la perte osseuse radiographique ?
Parce que la perte osseuse doit impliquer une étendue substantielle de la dimension vestibulo-lingual pour être visible radiologiquement. En effet, un défaut angulaire peut ne pas être détectable en raison de la superposition des corticales vestibulaires et linguales. Ainsi, les stades débutants de la parodontite ne seraient pas détectés. (Fig. 1)
Le diagnostic parodontal suit le schéma de classification défini lors de l'Atelier mondial de 2017 sur la classification des maladies et affections parodontales et péri-implantaires. La parodontite est caractérisée en fonction du stade et du grade de la maladie (basés sur le système de classification en oncologie) : le stade reflète la gravité, l'étendue et la répartition de la maladie, ainsi que la complexité anticipée de sa prise en charge. Le grade reflète d’autres dimensions biologiques de la maladie, notamment le taux de progression observé et/ou anticipé, les résultats prévus du traitement et le risque que la maladie ou son traitement nuise à l’état de santé général du patient.
Le stade, qui dépend de la gravité de la maladie et de la complexité anticipée de la prise en charge du cas, doit constituer la base du plan de traitement du patient, basé sur les preuves scientifiques des différentes interventions thérapeutiques. Le grade, qui fournit des informations complémentaires sur les facteurs de risque et le taux de progression de la maladie, devrait servir de base à la planification individuelle des soins.
Selon cette classification :
La santé parodontale clinique est définie par l'absence d'inflammation (mesurée par la présence d'un saignement au sondage (BOP) sur moins de 10 % des sites) et par l'absence de perte d'attache et de perte osseuse résultant d'une parodontite antérieure.
La gingivite est définie par la présence d'une inflammation gingivale, telle qu'évaluée par l’indice de saignement (BOP) sur ≥ 10 % des sites et par l'absence de perte d'attache détectable due à une parodontite antérieure. La gingivite localisée est définie par 10 à 30 % de sites avec saignement, tandis que la gingivite généralisée est définie par > 30 % de sites avec saignement.
La parodontite est définie par la perte du support parodontal, qui est généralement évaluée par une perte interproximale d'attache clinique mesurée au sondage et une perte osseuse radiographique. D'autres descriptions significatives de la parodontite incluent le nombre et les proportions de dents dont la profondeur de poche dépasse certains seuils (généralement profondeur de poche (PP) > 4 mm avec BOP ou PP≥ 6 mm), le nombre de dents perdues en raison d'une parodontite, le nombre de dents présentant des lésions intra-osseuses et la nombre de dents présentant des lésions inter-radiculaires. (Fig. 2 et 3)

Définitions des maladies péri-implantaires (Berglundh et al., 2018)
Une nouvelle classification de la santé et des maladies péri-implantaires a été proposée lors du Workshop de 2018.
La santé péri-implantaire est définie cliniquement et histologiquement : Cliniquement, elle se caractérise par une absence de signes visuels d'inflammation et de saignement ou de suppuration au sondage. La santé péri-implantaire peut exister autour d’implants avec un support osseux normal ou réduit. Il n’est pas possible de définir une gamme de profondeurs de sondage compatible avec la santé péri-implantaire. (Fig. 4)
La mucosite se caractérise par la présence de saignements (plus d'un point à un endroit autour de l'implant ou présence d'une ligne de saignement ou abondante) et/ou de suppuration au sondage doux avec ou sans augmentation de la PP par rapport aux examens précédents. Les niveaux osseux ne doivent, pas être modifiés au-delà des modifications crestales résultant du remodelage osseux initial. (Fig. 5)
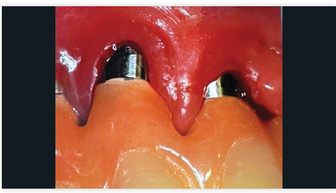
La péri-implantite (PI) est décrite comme un état pathologique associé à la plaque caractérisé par une inflammation de la muqueuse péri-implantaire et une perte progressive de l'os de soutien. Selon Berglundh et Schwartz (2018), le diagnostic de PI repose sur : la présence de saignement et/ou de suppuration au sondage doux, une augmentation de la PP par rapport aux examens précédents et la présence d’une perte osseuse au-delà des modifications du niveau crestal résultant du remodelage osseux initial. (Fig. 6 et 7)
Cependant, en l’absence de données d’examen préalable, le diagnostic de PI peut reposer sur la combinaison de : présence de saignement et/ou de suppuration au sondage doux + PP de ≥ 6 mm + perte osseuse ≥ 3 mm.
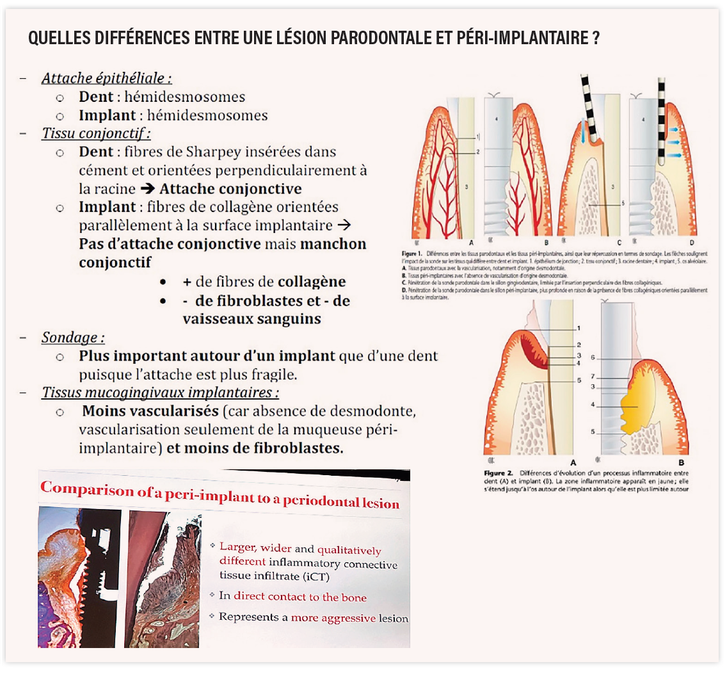
L’épaisseur des tissus mous et durs péri-implantaires est intimement liée à celle des tissus du site édenté avant implantation. Ainsi, des sites avec un déficit osseux important, un phénotype fin et une faible hauteur de tissus kératinisée sont plus à risque de récession muqueuse péri-implantaire. Une mauvaise position des implants, peut engendrer les mêmes conséquences.
Règles de base, précisions et zones « grises » de la classification de 2018 (Kornman et Papapanou, 2020)
La diffusion réussie de la nouvelle classification de la parodontite est facilitée par l'accent mis sur les règles de base, la clarification des ambiguïtés de l’ancienne classification et l'identification des « zones grises ». À l'heure de la médecine basée sur des données probantes et de la proposition de classifications pour guider certaines décisions thérapeutiques, il persiste des « zones grises » qui ne disposent pas de lignes directrices simples pour la prise de décision. Un sens/jugement clinique sera nécessaire pour poser le diagnostic dans certaines situations.
Les règles de base mises en évidences
- Le stade est un concept basé sur le patient et non sur la dent, par conséquent, un seul stade est attribué à chaque patient.
- Le stade peut augmenter avec le temps, si l'état parodontal se détériore, mais le stade initialement attribué est conservé même après une amélioration post-thérapeutique.
- Les facteurs de complexité qui déterminent le stade doivent être évalués collectivement pour parvenir à une évaluation cliniquement significative.
- Un seul grade est attribué à un patient sur la base d'une évaluation des tissus biologiques, en termes d'antécédents/risque de progression ultérieure, d'interaction des facteurs de risque et des effets bidirectionnels de la parodontite ou de son traitement sur l'état de santé général.
- Une évolution du grade est possible dans les 2 sens au fil du temps, après une évaluation approfondie et collective des changements dans les paramètres ci-dessus
Les zones grises incluent :
- un patient qui ne présente aucune perte osseuse radiographique avec une perte d'attache minimale à un âge avancé ;
- présence d’une atteinte parodontale affectant une seule dent (alors qu’il faut minimum 2 dents non adjacentes atteintes pour poser le diagnostic de parodontite) ;
- l'évaluation des facteurs qui conduisent/ne conduisent pas à une complexité accrue de la thérapie…
A retenir : il faut toujours évaluer le stade AVEC le grade (savoir si le patient est à risque majeur d’évolution ou pas) et ne PAS SOUS ESTIMER LE STADE I et II chez le jeune patient (ces cas nécessitent également une prise en charge spécifique)
Séquence pour le traitement des parodontites stade I à III (Sanz et al., 2020)
La première étape de la thérapeutique vise à guider le changement de comportement en motivant le patient à éliminer efficacement le biofilm dentaire supragingival et à contrôler les facteurs de risque.
Elle peut inclure les interventions suivantes :
- contrôle du biofilm dentaire supragingival,
- interventions pour améliorer l'efficacité de l'hygiène bucco-dentaire : motivation, instructions à l’hygiène orale,
- thérapies d'appoint pour l'inflammation gingivale,
- l'élimination mécanique professionnelle de la plaque dentaire, qui comprend des interventions professionnelles visant à éliminer la plaque supragingivale et le tartre, ainsi que les éventuels facteurs de rétention de plaque,
- contrôle des facteurs de risque, qui comprend toutes les interventions de changement de comportement en matière de santé éliminant/atténuant les facteurs de risque reconnus d'apparition et de progression de la parodontite (arrêt du tabac, contrôle métabolique amélioré du diabète et peut-être exercice physique, conseils diététiques et perte de poids).
Cette première étape thérapeutique doit être mise en œuvre chez tous les patients atteints de parodontite, quel que soit le stade de leur maladie, et doit être réévaluée fréquemment afin de : continuer à renforcer la motivation et l’adhésion, ou explorer d’autres alternatives pour surmonter les obstacles ; développer les compétences nécessaires à l’élimination du biofilm et favoriser une bonne réponse aux étapes thérapeutiques suivantes.
La deuxième étape de la thérapeutique vise à contrôler (réduire/éliminer) le biofilm sous-gingival et le tartre grâce à une instrumentation sous-gingivale. Cette étape thérapeutique doit être utilisée pour tous les patients atteints de parodontite, quel que soit le stade de leur maladie, seulement pour les dents présentant une perte de soutien parodontal et/ou une poche parodontale. Dans des situations cliniques spécifiques, comme en présence de sondages profonds, les premières et deuxièmes étapes du traitement peuvent être réalisées simultanément (par exemple pour prévenir le développement d'un abcès parodontal). La réponse individuelle à la deuxième étape du traitement doit être évaluée une fois les tissus parodontaux cicatrisés (réévaluation parodontale à 6 – 8 semaines). Si les critères d’évaluation du traitement (absence de poches parodontales > 4 mm avec saignement au sondage ou absence de poches parodontales profondes [≥ 6 mm]) n’ont pas été atteints, la troisième étape du traitement doit être envisagée. Si le traitement a réussi à atteindre les objectifs thérapeutiques, les patients doivent être placés dans un programme de thérapeutique de soutien.
La troisième étape du traitement vise à traiter les poches parodontales résiduelles (poches ≥4 mm avec saignement au sondage ou poches profondes ≥6 mm), dans le but d'accéder davantage à l'instrumentation sous-gingivale, de régénérer ou de réséquer les lésions qui ajoutent de la complexité à la prise en charge de la parodontite telles que les lésions intra-osseuses et inter-radiculaires.
Cela peut inclure les interventions suivantes :
- instrumentation sous-gingivale répétée avec ou sans thérapies d'appoint,
- lambeau d’assainissement,
- chirurgie parodontale résectrice,
- chirurgie parodontale régénératrice.
Lorsqu’il existe une indication d’intervention chirurgicale, elle doit être soumise au consentement supplémentaire du patient et une évaluation spécifique des facteurs de risque ou des contre-indications médicales doit être envisagée. La réponse individuelle à la troisième étape du traitement doit être réévaluée (réévaluation parodontale à 3 mois ou 6 mois si régénération parodontale). Idéalement, les objectifs du traitement doivent être atteints, et les patients doivent être placés en maintenance parodontale. Toutefois, certaines poches peuvent persister sur certaines dents chez les patients atteints de parodontite de stade III.
La thérapeutique parodontale de soutien vise à maintenir la stabilité parodontale chez tous les patients atteints de parodontite traités en combinant des interventions préventives et thérapeutiques définies dans les premières et deuxièmes étapes du traitement, en fonction de l'état parodontal du patient. Cette étape doit être effectuée à intervalles réguliers en fonction des besoins du patient, et lors de chacune de ces visites de rappel, tout patient peut avoir besoin d'un nouveau traitement si une récidive est détectée. Dans ces situations, un diagnostic et un plan de traitement appropriés doivent être établis à nouveau. De plus, le respect des mesures d’hygiène bucco-dentaire recommandés et un mode de vie sain font partie des soins parodontaux de soutien.
À n’importe quelle étape du traitement, l’extraction dentaire peut être envisagée si le pronostic des dents affectées est considéré comme sans espoir.
Parodontite de stade IV : besoin en réhabilitation complexe (Herrera et al., 2022)
La parodontite de stade IV est identifiée parmi la population plus large d'individus atteints de parodontite de stade III, définie par une inflammation parodontale et une perte d'attache atteignant le tiers moyen de la racine ou au-delà, en fonction de la nécessité d'une réhabilitation complexe en raison de la présence d'un ou plusieurs des facteurs suivants.
- Traumatisme occlusal secondaire/hypermobilité dentaire en raison d’un support parodontal réduit par la présence d’une parodontite stabilisée ou non,
- La migration dentaire, la dérive et l'ouverture de diastèmes associées à une perte d'attache importante au niveau des dents affectées,
- Perte de cinq dents ou plus due à une parodontite,
- Perte du calage postérieur et/ou évasement des dents antérieures dues à une parodontite,
- Perte de la fonction masticatoire (dysfonctionnement masticatoire) secondaire à une combinaison des éléments ci-dessus.
Les signes et symptômes de déficience fonctionnelle (dysfonction masticatoire) ci-dessus peuvent également être présents sous forme de séquelles de perte de dents multiples dues à une carie ou à une malocclusion grave chez des personnes sans atteinte parodontale significative ou même chez atteints de parodontite de stades I à II, qui ne répondent pas aux critères du stade IV. Le diagnostic différentiel est donc important.
La parodontite de stade IV affecte le pronostic de l’ensemble des dents. Chez ces patients, le contrôle de la parodontite (par le traitement parodontal standard, c'est-à-dire les étapes I à III puis des soins parodontaux de soutien) n'est pas suffisant pour stabiliser la maladie, résoudre la dysfonction masticatoire et améliorer la qualité de vie. Un plan de traitement interdisciplinaire pouvant inclure la prise en charge d'un traumatisme occlusal secondaire, une thérapeutique orthodontique et/ou des soins restaurateurs après une thérapeutique parodontale réussie doit donc être mis en œuvre pour traiter de manière optimale ces patients.
Bibliographie :
- Papapanou PN, Sanz M, Buduneli N, Dietrich T, Feres M, Fine DH, Flemmig TF, Garcia R, Giannobile WV, Graziani F, Greenwell H, Herrera D, Kao RT, Kebschull M, Kinane DF, Kirkwood KL, Kocher T, Kornman KS, Kumar PS, Loos BG, Machtei E, Meng H, Mombelli A, Needleman I, Offenbacher S, Seymour GJ, Teles R, Tonetti MS. Periodontitis: Consensus report of workgroup 2 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol. 2018 Jun;89 Suppl 1:S173-S182.
- Berglundh T, Armitage G, Araujo MG, Avila-Ortiz G, Blanco J, Camargo PM, Chen S, Cochran D, Derks J, Figuero E, Hämmerle CHF, Heitz-Mayfield LJA, Huynh-Ba G, Iacono V, Koo KT, Lambert F, McCauley L, Quirynen M, Renvert S, Salvi GE, Schwarz F, Tarnow D, Tomasi C, Wang HL, Zitzmann N. Peri-implant diseases and conditions: Consensus report of workgroup 4 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol. 2018 Jun;89 Suppl 1:S313-S318.
- Kornman KS, Papapanou PN. Clinical application of the new classification of periodontal diseases: Ground rules, clarifications and "gray zones". J Periodontol. 2020 Mar;91(3):352-360.
- Sanz M, Herrera D, Kebschull M, Chapple I, Jepsen S, Beglundh T, Sculean A, Tonetti MS; EFP Workshop Participants and Methodological Consultants. Treatment of stage I-III periodontitis-The EFP S3 level clinical practice guideline. J Clin Periodontol. 2020 Jul;47 Suppl 22(Suppl 22):4-60.
- Herrera D, Sanz M, Kebschull M, Jepsen S, Sculean A, Berglundh T, Papapanou PN, Chapple I, Tonetti MS; EFP Workshop Participants and Methodological Consultant. Treatment of stage IV periodontitis: The EFP S3 level clinical practice guideline. J Clin Periodontol. 2022 Jun;49 Suppl 24:4-71.