Procréation Médicalement Assistée et maladies parodontales
Dossier Maladies parodontales et pathologies générales : indissociables !
AO News # 51 - Juillet 2022
La procréation médicalement assistée (PMA) est un traitement médical utilisant des gamètes (ovule / spermatozoïde) pour favoriser l’obtention d’une grossesse. Les différentes techniques de PMA s’appuient toutes sur la stimulation ovarienne par traitement hormonal médicamenteux. Or, ces modifications hormonales, observées pendant la grossesse sur des périodes moins longues, sont susceptibles de provoquer ou d’aggraver des pathologies parodontales. Le lien de causalité entre pathologies inflammatoires parodontales et modifications hormonales durant la grossesse est aujourd’hui bien documenté (Bett et al. 2019). De même, le lien entre les modifications hormonales de la PMA et l’inflammation parodontale fait l’objet d’un nombre croissant d’études scientifiques.
La loi de bioéthique n°2021-‐1017 du 2 août 2021 a élargi l’accès à la procréation médicalement assistée aux couples de femmes et aux femmes célibataires. La PMA était auparavant réservée aux couples hétérosexuels, sur indication médicale et seulement en cas de diagnostic d’infertilité. En 2018, 148 711 tentatives de PMA ont été réalisées en France, engendrant 22,53% de grossesses et 18,91% d’accouchements, toute techniques de PMA confondues (Rapport médical et scientifique de l’agence de biomédecine 2019). L’élargissement des conditions d’accès à la PMA est susceptible d’augmenter le nombre de femmes en cours de traitement, et par conséquent d’augmenter la prévalence des problèmes parodontaux liés à ces traitements. Les dentistes et parodontistes vont donc être amenés à traiter un nombre croissant de pathologies parodontales liées aux modifications hormonales engendrées par la PMA. Nous proposons ici de faire le point sur les connaissances scientifiques et sur les recommandations de traitement face à une patiente en cours de PMA.
Les traitements de procréation médicalement assistée (PMA)
Il existe quatre principales techniques médicales de PMA. Toutes ces techniques recourent à la stimulation ovarienne par traitement hormonal médicamenteux. Ces traitements varient dans leur nature et leur durée, mais sont tous susceptibles d’altérer la santé parodontale (Lalasa et al. 2014).
L’insémination artificielle consiste à injecter du sperme traité, directement dans l’utérus d’une femme en période d’ovulation. Auparavant, la patiente a bénéficié d’un traitement de stimulation ovarienne, afin de maximiser les chances de succès.
La fécondation in vitro (FIV) permet de réaliser la fécondation d’un ovule et d’un spermatozoïde en laboratoire. La patiente reçoit généralement
une stimulation hormonale par de la FSH exogène (Follicule Stimulating Hormone) en quantité́ supérieure à celle utilisée pour l’insémination artificielle. (fig 1)
La FIV avec ICSI ou IMSI : la FIV peut être utilisée avec deux techniques complémentaires. La FIV avec ICSI (Intra-‐Cytoplasmic Sperm Injection) consiste à injecter le spermatozoïde directement dans l’ovocyte. Enfin, la FIV avec IMSI (Intra-‐ Cystoplasmic Morpholigically-‐Selected Sperm Injection) permet de sélectionner par microscopie les spermatozoïdes utilisés. (fig 2)
L’accueil d’embryon est la dernière technique : un couple stérile, ou à risque de transmission de maladie génétique, peut demander à recevoir un embryon congelé́ issu d’un autre couple. La femme concernée subit préalablement une hormonostimulation pour l’accueil de l’embryon. Celui-‐ci est ensuite introduit dans son utérus.


Quelle que soit la technique utilisée, des traitements hormonaux sont administrés concomitamment aux femmes en cours de PMA. Les objectifs sont doubles : favoriser le développement de plusieurs follicules (contenant les ovocytes), et limiter les ovulations spontanées.
Les protocoles sont variables selon la technique et la patiente, mais comprennent tous trois phases.
Phase de stimulation : la première phase des traitements hormonaux au cours de la PMA consiste à stimuler les ovaires pour obtenir la croissance de plusieurs follicules. Les médicaments administrés sont à base de FSH. La FSH est une hormone folliculostimulante hypophysaire. Un suivi est réalisé, grâce à des dosages répétés de l’œstradiol. L’œstradiol est une hormone, qui est produite par les ovaires et les surrénales. Les dosages obtenus doivent être compris entre 200 à 500 ng/L pour l’insémination artificielle et entre 1500 à 4500 ng/L pour les FIV, IMSI et ICSI.
Phase de blocage : la deuxième phase a pour but d’éviter de perdre des ovocytes. Les médicaments utilisés permettent de bloquer la production hypophysaire de gonadotrophines, hormones stimulant l’activité ovarienne.
Phase de déclenchement de l’ovulation : la troisième phase permet de contrôler le moment de déclenchement de l’ovulation. On recoure pour cela à une injection unique d’hCG : la gonadotrophine chorionique humaine est une hormone produite par le placenta de la femme enceinte.
Ainsi, ces traitements sont basés sur des hormones naturellement produites par une femme en cours d’ovulation ou enceinte. Ils modifient les taux d’hormones circulantes, tout comme une grossesse naturelle. Les dosages ne sont toutefois pas comparables : par exemple, le pic d’œstradiol au terme de la grossesse atteint 30000 ng/L contre 4500 ng/L au maximum pour une FIV. Cependant, ces modifications, souvent répétées plusieurs fois, pourraient être susceptibles d’avoir des répercussions parodontales, tout comme une grossesse naturelle.
Effets des hormones sexuelles sur le parodonte
Les hormones sexuelles circulantes agissent sur les tissus cibles grâce à des récepteurs spécifiques situés dans ces tissus. Les organes cibles sont nombreux, et les principaux sont les organes sexuels : par exemple, le contrôle des flux sanguins dans l’utérus au cours des cycles menstruels et au cours de la grossesse dépend du taux d’œstrogènes circulants.
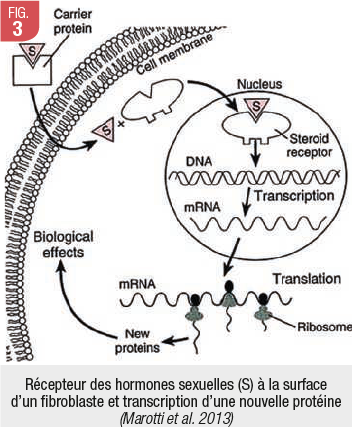
Étonnamment, les hormones sexuelles, dont notamment les œstrogènes, ont également une myriade d’effets sur le parodonte (Marotti et al. 2013). En effet, le ligament dentaire contient des fibroblastes qui expriment de nombreux récepteurs à grande affinité pour les œstrogènes. C’est pourquoi le parodonte est un tissu cible privilégié de ces hormones. Une fois liée à la cellule, l’hormone permet la transcription d’une nouvelle protéine (Fig. 3), qui aura plusieurs effets sur le parodonte environnant.
Le métabolisme de ces hormones dans le parodonte emprunte alors différentes voies. On peut brièvement citer les effets suivants : elles modifient la pathogénicité des micro-organismes voisins, elles augmentent la perméabilité des capillaires, elles modifient la production de cytokines, modulant ainsi la réponse inflammatoire, et enfin elles diminuent l’efficacité des polymorphonucléaires. Ces mécanismes biologiques expliquent la majoration de l’inflammation parodontale observée au cours de la grossesse, et donc de la PMA également (Fig. 4).

Association PMA et pathologies parodontales
Ceci étant, la compréhension des mécanismes biologiques est insuffisante pour prouver un lien de causalité en médecine. Il faut pour cela disposer aussi d’études prospectives contrôlées de suivi, de bonne qualité méthodologique et avec des cohortes de patientes suffisantes. Une revue de littérature, réalisée dans le cadre de la thèse d’exercice du Dr Audrey Seroka, soutenue en 2018 (Seroka 2018), a synthétisé les données de six études cliniques. Ces études cliniques permettent d’établir un lien bidirectionnel entre PMA et pathologies parodontales.
Corrélation PMA et inflammation parodontale
Plusieurs études de cohorte ont comparé les indices d’inflammation parodontale de femmes en cours de PMA avec un groupe témoin de femmes qui ne suivaient pas ce traitement (Lalasa et al. 2014, Haytaç et al. 2004, Vasudevan et al. 2013). Les résultats congruents de ces études permettent d’établir un lien de causalité entre PMA et inflammation parodontale : les traitements hormonaux de la PMA majorent l’inflammation parodontale des femmes en cours de traitement.
De plus, à indice de plaque égal, c’est-‐à-‐dire quel que soit le niveau d’hygiène orale des patientes, l’inflammation est également majorée lors du traitement de PMA (Smadi et al. 2017). La prise en compte de l’indice de plaque des patientes permet d’éliminer un biais : les femmes des groupes tests auraient pu avoir une moins bonne hygiène que les femmes des groupes témoins, ce qui aurait remis en cause l’association entre PMA et inflammation parodontale, mais ce n’est pas le cas.
Une étude s’est en outre intéressée à l’effet de la PMA sur des femmes selon leur statut parodontal initial (Pavlatou et al. 2013) : si la PMA aggrave l’inflammation chez toutes les femmes, cette aggravation est plus marquée chez les femmes présentant une inflammation parodontale préexistante (gingivite). Cette étude montre également que l’association inverse est vraie : les femmes initialement atteintes de gingivite ont eu de moins bons résultats pour leur FIV.
Durée de l’inflammation et périodes à risque
Comme nous l’avons vu, le traitement hormonal administré pendant la PMA comprend différentes phases. Une étude montre que plus la durée de la PMA augmente (et notamment, plus le nombre de tentatives nécessaires pour obtenir une grossesse est grand), plus l’inflammation parodontale est majorée (Haytaç et al. 2004). Toutefois, on ne peut pas aujourd’hui discerner une phase spécifique de la PMA comme étant plus à risque d’aggraver l’inflammation parodontale qu’une autre.
Effets du détartrage sur l’inflammation parodontale
Une étude a comparé l’effet du détartrage chez des femmes en cours de PMA avec un groupe contrôle de femmes non traitées (Vasudevan et al. 2013). Avant détartrage, les femmes en cours de PMA avaient une inflammation parodontale supérieure à celles du groupe contrôle. Après détartrage, toutes les femmes ont bénéficié d’une diminution de l’inflammation.
Toutefois, les femmes du groupe test ont conservé une inflammation plus élevée, alors que les femmes du groupe contrôle ont bénéficié grâce au détartrage d’une résolution complète de leur inflammation. Ainsi, le détartrage est un traitement efficace pour diminuer l’inflammation, mais ne suffit pas à endiguer complétement l’inflammation parodontale des femmes en cours de PMA.
Effets indirects de la PMA sur l’inflammation parodontale
Enfin, au-‐delà de l’effet direct des médicaments hormonaux sur l’inflammation parodontale, l’étude de la littérature permet de déceler deux effets indirects : xérostomie et stress. Une étude comparative a mis en évidence une xérostomie observée chez 95% de patientes en cours de PMA (Giura et al. 2012). Or, la sécheresse buccale majore le risque de problèmes parodontaux. Toutefois, le protocole de l’étude est incomplètement décrit dans l’article, le nombre de participantes n’est pas précisé, et la méthode statistique utilisée n’est pas décrite. Ainsi, cette étude ne permet pas de conclure à une association entre PMA et xérostomie, les preuves scientifiques faisant défaut. Mais elle permet d’attirer l’attention des cliniciens sur le risque de xérostomie pendant la PMA.
Enfin, le facteur stress est mentionné dans une étude (Haytaç et al. 2004). Le stress est connu en parodontie pour avoir un impact direct sur l’inflammation parodontale via des médiateurs biochimiques circulants, et également un effet indirect en majorant les comportements à risque (augmentation du tabagisme et diminution de l’hygiène dentaire). Ainsi, comme pour la xérostomie, l’association entre PMA et stress souffre d’un défaut de preuves scientifiques, mais la connaissance de ce lien possible peut influer sur la prise en charge des patientes en cours de PMA.
Recommandations pour la prise en charge parodontale de patientes en cours de PMA
Dépistage des femmes en cours de PMA au cabinet dentaire
L’association entre PMA et pathologies parodontales est aujourd’hui peu connues par les patientes. Ainsi, une patiente qui consulte pour un problème parodontal au cabinet dentaire ne mentionnera pas systématiquement qu’elle est en cours de PMA. Aussi, la première mesure à prendre est certainement d’ajouter une question au questionnaire médical : à la suite de la question êtes-‐vous enceinte ? On peut simplement ajouter êtes-‐vous en cours d’assistance médicale à la procréation ?
La Fédération Européenne de Parodontie va même un peu plus loin (Recommandations EFP 2020), en incitant les praticiens à demander à toute femme en âge de procréer si elle a un projet de grossesse. Une prévention des pathologies parodontales qui peuvent advenir au cours de la grossesse peut ainsi être réalisée. Et les potentielles parturientes peuvent ainsi aborder leur grossesse avec un parodonte en parfaite santé.
Motivation des patientes en cours de PMA
En santé publique, le fait que les femmes enceintes sont particulièrement réceptives aux messages d’éducation à la santé orale est bien identifié : la Sécurité Sociale propose à toute femme enceinte une consultation de dépistage des éventuels problèmes dentaires et parodontaux. Un tel mécanisme n’est aujourd’hui pas proposé aux femmes en cours de PMA. On pourrait pourtant penser que ces femmes sont dans une disposition d’esprit similaire au regard de l’éducation à la santé. Ainsi, les messages suivants sont susceptibles de retenir l’attention des femmes en cours de PMA.
Messages à délivrer aux femmes en cours d’assistance médicale à la procréation
- les modifications hormonales de la PmA, comme celles de la grossesse, majorent l’inflammation et aggravent les pathologies parodontales.
- l’inflammation gingivale peut engendrer des dégâts irréversibles sur les tissus parodontaux, mais aussi des complications de la grossesse, ainsi qu’une diminution
du taux de succès de la PmA.
- il ne faut pas hésiter à consulter au moindre symptôme (inflammation et saignements des gencives notamment). - la plupart des traitements parodontaux sont
possibles durant la PmA et la grossesse.
Des auteurs américains ont pu montrer que l’assertion populaire, selon laquelle chaque grossesse faisait perdre une dent, était contre toute attente vraie, d’un point de vue épidémiologique aux États-‐Unis. Selon eux, ce fait serait en partie dû à l’aggravation des problèmes parodontaux au cours de la grossesse (Figuero et al. 2013). Ainsi, les femmes primipares, que leur grossesse soit naturelle ou inscrite dans une démarche de PMA, doivent être informées qu’une prévention des problèmes parodontaux fréquemment rencontrés au cours de la grossesse permet d’éviter de nombreuses complications.
Traitement parodontal des femmes en cours de PMA
Pour l’heure, il n’existe pas de recommandations professionnelles spécifiques pour la prise en charge des femmes en cours de PMA. Toutefois, les modifications hormonales étant comparables à celles observées pendant la grossesse, les recommandations s’approchent de celles données pour la femme enceinte, exception faite de toutes les restrictions liées à la tératogénicité des traitements.
La motivation à l’hygiène buccodentaire est essentielle, comme pour tout patient pris en charge en parodontie. La technique de brossage peut être adaptée à la majoration de l’inflammation. La dureté des poils de la brosse à dents peut être diminuée pour limiter l’inconfort du brossage en présence de gencives inflammatoires.
Le diagnostic clinique et radiographique peut et doit être fait. Les radios sont en effet déconseillées pendant la grossesse, le bilan long cone gagnera donc à être réalisé en amont de la grossesse à venir.
La thérapeutique non chirurgicale par détartrages et surfaçages est sûre et efficace pendant la PMA et pendant la grossesse (Recommandations EFP 2020). Les séances nécessaires seront réalisées comme pour une patiente non enceinte et n’étant pas en cours de PMA.
La réévaluation sera réalisée selon les recommandations habituelles. Un sondage complet, un relevé des indices de saignements et de plaque seront réalisés environ 6 semaines après le dernier surfaçage (Segelnick et al. 2006).

Les chirurgies parodontales pourront être réalisées, en gardant à l’esprit qu’elles restent déconseillées pendant le premier trimestre de la grossesse. Il faut donc veiller à les programmer à distance de la troisième phase de la PMA, au moment où la patiente a de grandes chances de tomber enceinte. De plus, les possibilités de prescription sont également limitées pendant la grossesse (recommandations EFP 2020), il est donc préférable de ne pas être en phase de cicatrisation au moment du début de la grossesse.
La maintenance parodontale et le monitoring enfin seront un peu plus fréquent pendant toute la durée de la PMA et de la grossesse. A ce jour, il n’existe pas de recommandations spécifiques pour la fréquence de la maintenance parodontales chez les femmes en cours de PMA. Toutefois, nous avons vu que même après détartrage, l’inflammation avait tendance à persister chez ces femmes. Or l’inflammation, et notamment le saignement au sondage, est un paramètre retrouvé dans tous les modèles proposant de définir une fréquence de maintenance en fonction des facteurs de risque (Lang et al.2015). Ainsi, la majoration de la fréquence de la maintenance est nécessaire, et sera appréciée par le praticien au cas par cas.
Conclusions
Malgré le faible nombre d’études sur PMA et pathologies parodontales, l’association bidirectionnelle entre inflammation gingivale et traitements hormonaux au cours de la PMA est aujourd’hui bien établie. Les femmes entamant une démarche de PMA gagnent donc à être informées des risques pour leur parodonte, mais aussi du fait qu’une parodontite non traitée diminue les chances d’obtenir une grossesse par la PMA. Ainsi, les traitements parodontaux sont non seulement possibles, mais aussi souhaitables au cours de la PMA. Les praticiens peuvent désormais les mener sereinement grâce aux publications et aux preuves scientifiques croissantes sur le sujet.
BIBLIOGRAPHIE
Bett et al.. 2019 Prevalence of oral mucosal disorders during pregnancy : a systematic review and meta-¬‐analysis. J. Oral. Pathol. Med. 2019 Apr;48(4):270-¬‐277.
Figuero et a. 2013. Pregnancy gingivitis and causal inference. J. Clin. Periodontol. 2013;40:457-¬‐473.
Giura & Dumitriu 2012 Preliminary clinical observations on the gingival-¬‐periodontal manifestations in in vitro fertilized female patients. International Journal of Medical Dentistry 2012. Vol 2, page 107-¬‐ 111.
Haytaç et al.. 2004 The effects of ovulation induction during infertility treatment on gingival inflammation. J Periodontol. 2004 Jun;75(6):805-¬‐10.
Lalasa et al.. 2014 Periodontal status in infertile women attending in vitro fertilization clinics. Indian J Dent Res. 2014 Jan-¬‐Feb;25(1):50-¬‐3.
Lang et al.. 2015 Risk factor assessment tools for the prevention of periodontitis progression a systematic review. J Clin Periodontol 2015;42(Suppl. 16):S59-¬‐S70.
Marotti & Mawhinney 2013 Endocrinology of sex steroid hormones and cell dynamics in the periodontium. Perio 2000, vol. 61, 2013, 69-¬‐88.
Pavlatou et al.. 2013 The effect of in vitro fertilization on gingival inflammation according to women’s periodontal status: clinical data. J Int Acad Periodontol. 2013 Apr;15(2):36-¬‐42.
Rapport médical et scientifique de l’agence de biomédecine 2019. Assistance médicale à la procréation – les chiffres clés. https://rams.agence-¬‐biomedecine.fr/principaux-¬‐chiffres-¬‐de-¬‐ lactivite
Recommandations de l’European Federation of Periodontology (EFP) pour les praticiens prenant en charge des femmes enceintes. Mars 2020. https://www.efp.org/fileadmin/uploads/efp/Documents/CPMAaigns/Oral_Health_and_Preg nancy/Brochures/key-¬‐messages-¬‐dental.pdf
Segelnick & Weinberg 2006 Reevaluation of initial therapy : when is the appropriate time? J Periodontol 2006 Sep;77(9):1598-¬‐601.
Seroka 2019 Analyse de l’état de santé parodontale chez les femmes ayant recours à la procréation médicalement assistée. Thèse pour le diplôme d’État de Docteur en Chirurgie Dentaire. Paris VII Diderot 2019.
Smadi 2017 Gingival and periodontal changes in patients undergoing in vitro fertilization treatment: A clinical study. Indian J Dent Res. 2017 Nov-¬‐Dec;28(6):650-¬‐654.
ICONOGRAPHIE
FIGURE 1 Les différentes étapes de la Fécondation In Vitro (FIV). https://www.inserm.fr/dossier/assistance-¬‐medicale-¬‐procreation-¬‐PMA/
FIGURE 2 Fécondation In Vitro avec ICSI (Intra-¬‐cytoplasmic Sperm Injection). https://www.inserm.fr/dossier/assistance-¬‐medicale-¬‐procreation-¬‐PMA/
FIGURE 3 Récepteur des hormones sexuelles (S) à la surface d’un fibroblaste et transcription d’une nouvelle protéine (Marotti et al.. 2013)
FIGURE 4 Vue clinique de la réévaluation d’une patiente en cours de PMA.
