Diagnostic et prise en charge d’une lésion kystique mandibulaire
Samy Tawfik, Nathan Moreau
Dossier spécial Médecine et Chirurgie Orale - AO News #34-35 Juin/Juillet 2020

Introduction
Les lésions kystiques des mâchoires sont un motif fréquent de consultation (et d’adressage) en chirurgie orale (1). La grande majorité de ces kystes sont d’origine infectieuse, résultant d’une prolifération épithéliale autour d’un tissu de granulation péri-apical. Dès lors que cette prolifération épithéliale s’organise, elle va évoluer pour son propre compte et posséder un caractère expansif lent et progressif (du fait de l’augmentation importante de la pression osmotique intra-kystique) pouvant refouler les structures adjacentes telles que le nerf alvéolaire inférieur à la mandibule (2). Ceci devra être pris en compte lors de l’intervention pour éviter d’éventuelles complications neurologiques (hypoesthésies, paresthésies, dysesthésies, voire douleurs neuropathiques) souvent très invalidantes (2). Par ailleurs, les examens radiographiques (dont un examen tridimensionnel) s’attacheront à objectiver les critères de bénignité et d’agressivité de la lésion afin de choisir la meilleure conduite à tenir chirurgicale prenant en compte à la fois le délabrement osseux nécessaire et le risque de récidive de la lésion (3). Du fait de la présentation radiographique souvent non spécifique des kystes des mâchoires, ce sera l’examen anatomopathologique –obligatoire sur le plan médico-légal– qui permettra d’obtenir le diagnostic étiologique de la lésion kystique (3).
Observation clinique
Un patient de 48 ans, en bonne santé générale, a été adressé à la consultation de chirurgie orale par son chirurgien-dentiste, suite à deux épisodes infectieux mandibulaires droits. La radiographie panoramique réalisée par le praticien objectivait une volumineuse image lacunaire radio-claire bien délimitée appendue aux apex de la 46, semblant refouler le canal mandibulaire, restant à distance du rebord basilaire inférieur. Une radio-opacité longiligne au niveau de l’apex de la racine mésiale de 46 était évocatrice d’un dépassement péri-apical d’un instrument fracturé (Fig. 1).
L’examen clinique réalisé lors de la consultation était sans particularité. En outre, aucune déformation osseuse, fistule cutanée ou muqueuse, ainsi qu’aucune altération de la sensibilité trigéminale n’étaient retrouvés. Aucune lésion muqueuse en regard de la lésion kystique n’était objectivée non plus.
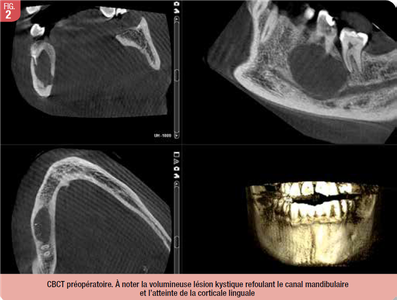
Un examen complémentaire d’imagerie tridimensionnelle CBCT a été réalisé pour compléter le bilan d’imagerie et objectiver les rapports de la lésion d’allure kystique avec le canal mandibulaire et les parois osseuses mandibulaires. Ce dernier retrouvait une lacune radio-claire de tonalité homogène, de 2 cm de diamètre, autour des racines de 46 dont l’aspect était fortement évocateur d’un kyste inflammatoire péri-apical. L’analyse des coupes coronales permit de mettre en évidence une atteinte de la corticale linguale dans sa partie inférieure basale ainsi qu’un refoulement du canal mandibulaire en regard (Fig. 2). Au total, l’aspect radiographique était compatible avec un kyste inflammatoire péri-apical sans signe majeur d’agressivité (hormis l’atteinte de la corticale linguale mais dont l’aspect homogène était rassurant dans ce contexte).
Après avis d’un endodontiste, ayant jugé le retraitement endodontique irréaliste dans le présent cas, il a été décidé de procéder à l’avulsion de la dent et de réaliser l’énucléation de la lésion kystique par voie trans-alvéolaire élargie (facilitée par l’alvéolyse préexistante).
Une prémédication antibiotique (amoxicilline 2g/jour pendant 5 jours à commencer la veille de l’intervention) et anti-inflammatoire (prednisone 80 mg/jour pendant 4 jours à commencer la veille de l’intervention) a été instaurée afin de limiter le risque de paresthésies/dysesthésies post-opératoires du fait de l’œdème chirurgical.

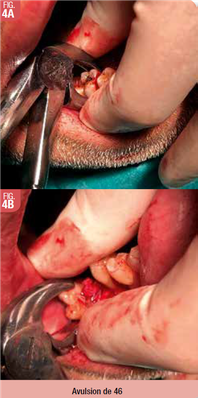
Après anesthésie loco-régionale (bloc du nerf alvéolaire inférieur) et infiltration du nerf buccal, un lambeau trapézoïdal a été récliné en vestibulaire de 46 avec une décharge en mésial de 45 (en prenant soin de ne pas léser le pédicule mentonnier) et une décharge distale le long de la ligne oblique externe (Fig. 3). La 46 a été luxée puis avulsée sans difficulté notable (Fig. 4). L’analyse peropératoire de la dent a permis d’objectiver l’instrument fracturé (Fig. 5A) et la résorption concave de la paroi linguale de la racine mésiale (Fig. 5B).


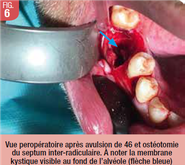
Afin de préparer l’énucléation du kyste sous-jacent, une ostéotomie du septum inter-radiculaire a été pratiquée, révélant la membrane kystique sous-jacente (Fig. 6). Puis une ostéotomie de la table osseuse vestibulaire a été réalisée selon un rectangle de 5 mm de hauteur par 10 mm de largeur, à l’aide d’une fraise boule sur pièce à main (Fig. 7), en veillant à ne pas léser la muqueuse kystique sous-jacente (afin de préserver l’intégrité de la membrane kystique). Les bords osseux ont ensuite été régularisés pour limiter tout risque de déchirement de la membrane kystique lors de l’énucléation.
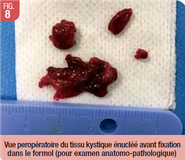
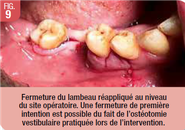
L’énucléation du kyste a été conduite par voie trans-alvéolaire élargie, à l’aide d’une curette de Lucas, en décollant la membrane kystique des différentes parois cavitaires, exception faite de la région linguale inférieure (où se situaient la fenestration osseuse et le nerf alvéolaire inférieur). Une fois le décollement subtotal, la pièce opératoire a pu être tractée hors de la cavité osseuse (Fig. 8), se décrochant sans difficulté au niveau de la région (à risque) non décollée. Celle-ci a été immédiatement fixée dans une solution de Formol à 10% puis envoyée au laboratoire d’anatomopathologie. Le site opératoire a été fermé en première intention avec des points discontinus au VICRYL 4-0 (Fig. 9).
Un contrôle de cicatrisation réalisé à 7 jours montrait une fermeture parfaite du site opératoire sans signe infectieux ou inflammatoire notable. Les douleurs post-opératoires ont été minimes.
L’analyse anatomopathologique de la pièce opératoire concluait à un kyste inflammatoire d’origine endodontique (lié à l’infection péri-apicale de 46).
Un contrôle radiographique est prévu à 6 mois (puis 1 an si nécessaire) pour contrôler la ré-ossification de la cavité osseuse résiduelle puis planifier la future réhabilitation prothétique.

Discussion
L’énucléation de kystes des mâchoires est un geste fréquent en chirurgie orale, reposant sur certains principes fondamentaux tels que le décollement puis l’élimination de toute la membrane kystique (parfois via un curetage appuyé au niveau des parois osseuses résiduelles), l’obtention d’un caillot sanguin occupé la totalité de la cavité osseuse résiduelle, ainsi qu’une fermeture primaire étanche en zone osseuse saine, sans fils de sutures suspendus au dessus de la cavité (1,4).
L’analyse rigoureuse de l’imagerie tridimensionnelle est un prérequis indispensable avant tout geste chirurgical d’énucléation kystique, en particulier lorsque la lésion kystique est proche et/ou refoule les structures nobles vasculo-nerveuses. Cette analyse permet d’anticiper au mieux les difficultés chirurgicales et permettrait potentiellement d’évoquer certains diagnostics selon –par exemple– la direction du refoulement du nerf alvéolaire inférieur par la lésion (3), même si une telle hypothèse mérite plus ample confirmation.
La question du comblement de la cavité osseuse résiduelle est fréquemment posée, notamment par les jeunes praticiens. En l’état actuel des connaissances scientifiques, il n’existe aucun argument en faveur du comblement de la cavité osseuse par un quelconque matériau qu’il soit (5,6) hormis le caillot sanguin (4), vraisemblablement le meilleur « matériau » de comblement.
Conclusion
Les kystes inflammatoires d’origine dentaire sont des entités fréquemment rencontrées en pratique quotidienne de chirurgie orale.
La connaissance des critères clinico-radiographiques de bénignité et d’agressivité est essentielle à la planification et à la réalisation du geste chirurgical.
Par ailleurs, une étroite collaboration entre le chirurgien-dentiste et le chirurgien oral doit permettre une prise en charge optimale de ces lésions parfois volumineuses et symptomatiques. Enfin, à l’instar de toute lésion tissulaire, un examen anatomopathologique est obligatoire tant sur le plan diagnostic que médico-légal.
Références bibliographiques
(1) Van Doorn ME. Enucleation and primary closure of jaw cysts. Int J Oral Surg 1972;1:17-25
(2) Han YS, Lee H, Seo BM. Fate of mandibular canals displaced by enlarged cystic lesions: does the inferior alveolar neurovascular bundle relocate to its original position? Br J Oral Maxillofac Surg. 2018;56:292-298.
(3) Kolokythas A, Al-Ghamian H, Miloro M. Does a difference exist in inferior alveolar canal displacement caused by commonly encountered pathologic entities? An observational study. J Oral Maxillofac Surg. 2011;69:1944-1951.
(4) Chiapasco M, Rossi A, Motta JJ, Crescentini M. Spontaneous bone regeneration after enucleation of large mandibular cysts: a radiographic computed analysis of 27 consecutive cases. J Oral Maxillofac Surg. 2000;58 (9):942-948.
(5) Ettl T, Gosau M, Sader R, Reichert TE. Jaw cysts – filling or no filling after enucleation? A review. J Craniomaxillofac Surg. 2012;40(6):485-93.
(6) Buchbender M, Neukam FW, Lutz R, Schmitt CM. Treatment of enucleated odontogenic jaw cysts : a systematic review. Oral Surg oral Med Oral Pathol Oral Radiol. 2018;125(5):399-406.
Retour au Dossier Médecine et Chirurgie Orale - AO#34-35 Juin/Juillet 2020