Réflexions sur la péri-implantite
Dossier Spécial 25 ans - AONews #30 - Novembre 2019

Les problèmes liés à cette pathologie sont constitués d’une part, par la difficulté inhérente aux traitements et d’autre part, par leur taux de succès aléatoire. En effet, les protocoles thérapeutiques proposés aujourd’hui, s’ils commencent à donner des résultats autorisant la réosséointégration des implants, restent complexes à mettre en œuvre et impliquent de combiner de multiples méthodes pour un résultat efficace. La vraie solution passe donc essentiellement par la prévention.
La prévention devient absolument prioritaire pour plusieurs raisons.
La prévalence de la péri-implantite serait de 10 % des implants et de 20 % des patients après 5 à 10 ans. Il s’agit d’une maladie multifactorielle (Mombelli A, Müller N, Cionca N. The epidemiology of peri-implantitis. Clin Oral Implants Res. 2012;23). Les facteurs de risque sont connus: HBD insuffisante, maladie parodontale, diabète, tabac…
La maladie parodontale concerne en moyenne, 50 % de la population adulte. Sa prise en charge s’impose avant toute pose d’implant car ces patients présentent une grande susceptibilité aux bactéries pathogènes susceptibles de déclencher une péri-implantite. La parodontite « chronique de l’adulte » ne constitue pas une contre-indication au traitement implantaire mais impose un traitement préalable et la mise en place de règles de maintenance strictes.
Il y a 13 millions d’utilisateurs réguliers de tabac en France et la péri-implantite est observée chez plus de 36 % des fumeurs (The Frequency of Peri-Implant Diseases: A Systematic Review and Meta-Analysis. Momen A. Atieh,* Nabeel H.M. Alsabeeha,† Clovis Mariano Faggion Jr.,* and Warwick J. Duncan*, J Periodontol 2013;84).
Il y a plus de 3 millions de diabétiques en France dont une partie non négligeable présente une altération du métabolisme exposant davantage aux processus infectieux. Hérédité, alcool, stress, dépression, sont autant de facteurs influençant de près ou de loin l’état de santé général et pouvant compliquer le tableau initial. En outre, il y a de plus en plus de praticiens poseurs d’implants débutants en France et ils n’ont pas suffisamment pris conscience de ces facteurs de risque.
La notion de facteur de risque accompagne celle des taux de succès implantaires. Un praticien débutant mettra un temps certain à connaître le taux de succès de 96 % habituel annoncé dans la littérature et qui concerne que des praticiens entraînés, expérimentés. Il se situera plutôt dans les 80-90 % et encore ne parle-t-on là que de succès à court terme. Alors que se passera-t-il au bout de 5-10 ans de pratique, lorsque la péri-implantite concernera 10 % des implants posés ? Comment expliquera-t-on aux patients que les microbes ont attaqué leur os alors que le succès à long terme leur avait été assuré au départ ? Qui payera les pots cassés ? Il sera alors bien temps de regretter d’avoir parlé de « garantie à vie ».
« La correction des facteurs ayant favorisé la survenue de la péri-implantite est indispensable pour éviter la récidive rapide ». P. Russe, P. Missika. Recommandations de bonnes pratiques en odonto-stomatologie. Espace ID 2015. Ne nous y trompons pas. Dans une société de plus en plus procédurière, les patients recherchent la responsabilité des praticiens, et le défaut d'information sur ce sujet leur permettra quelques confortables indemnités. Alors, sans doute, le Sou médical et plus généralement les assureurs de santé mettront le Holà et demanderont à l'Ordre ou au Ministre en charge de reprendre la main et de limiter la pratique implantaire aux praticiens dûment formés par l'Université. A défaut, nos primes d'assurance connaîtront un bond historique et c'est encore nous qui serons mis à l’index.
Alors que faire ?
Une seule réponse possible : modifier notre message et donner à chaque patient une information objective correspondant à son profil médico-dentaire. Aborder le sujet de la péri-implantite dès le début du plan de traitement s’impose. Le consentement éclairé doit comporter les informations sur l’obligation d’un suivi adapté et d’une hygiène quotidienne efficace faute de quoi le risque de développer la maladie péri-implantaire se réalisera. Compte tenu de ce qui a été dit précédemment, le diagnostic de la parodontite, quand elle existe, et sa prise en charge, devra représenter le premier acte de ce traitement implantaire. L’usage du tabac sera présenté comme un risque majoré imposant une prise en charge et des contrôles plus assidus.
Les relations entre péri-implantites et parodontites
Les maladies parodontales sont des maladies dont l’étiologie est plurifactorielle (mauvais contrôle de plaque génétique, immunitaire, pathologie générales associées etc …) mais dont le facteur bactérien est essentiel. Face à une parodontite avancée avec une alvéolyse plus ou moins sévère la réponse reste trop souvent l’extraction. Combien de fois, au cours de congrès, des conférenciers, soi-disant spécialistes, présentent des cas où bon nombre des dents extraites pourraient être conservé. Une des premières questions est de savoir si l’extraction règle de façon radicale la parodontite et le problème bactérien.
La réponse est non pour plusieurs raisons :
- en cas de parodontite sévère, des bactéries pathogènes pénètrent dans les tissus muqueux et osseux et ne sont ainsi pas éliminées par l’extraction ;
- en phénomène bien connu des parodontistes est celui de la translocation bactérienne à partir des poches profondes vers d’autres sites dentaires ou implantaires. (Matuliene et coll. 2008 ; Papaioannou et coll. 1995) ;
- même chez un patient totalement édenté la charge bactérienne n’est jamais nulle. Les muqueuses, la langue, les amygdales sont des réservoirs de bactéries très importants. (Danser et coll. 94 ; Van Assche et coll. 2009)
La réponse à une parodontite même très sévère ne peut donc être systématiquement l’extraction. Le seul moyen de réduire la charge bactérienne reste le traitement parodontal y compris pour des dents dont le pronostic est mauvais. La thérapeutique initiale reste ainsi fondamentale pour réévaluer la réponse tissulaire et la collaboration du patient (ce qui peut être riche d’enseignement pour la suite du traitement). Il conviendra d’être très prudent pour un traitement prothétique ou implantaire complexe vis-à-vis d’un patient peu coopérant ou peu performant au contrôle de plaque. En cela aussi l’approche parodontale à laquelle nous sommes habitués, permet de réorienter un traitement en fonction des différents résultats de la thérapeutique initiale. Certains pensent garantir leur traitement ou leurs extractions avec une prescription antibiotique.
Malheureusement là aussi, on risque de grandes déconvenues et pour plusieurs raisons :
- nous savons tous que les antibiotiques sont de moins en moins efficaces. Nous sommes confrontés à de plus en plus de phénomène de résistance et une panoplie de molécules relativement restreinte. Il faut garder les antibiotiques pour des indications précises (parodontites agressives, parodontites terminales entre autre) et toujours en accompagnement des thérapeutiques locales ;
- les bactéries pathogènes au sein du biofilm sont beaucoup plus résistantes que les bactéries en suspension dans la salive ou dans le fond des poches parodontales. De plus les bactéries ne sont pas pathogènes par elles-mêmes, mais sous forme de complexes (Socranski et coll. 98). Pour que les antibiotiques soient efficaces il est indispensable de désorganiser ce biofilm. De ce point de vue on en revient toujours au détartrage-surfaçage.
Une grande question reste de savoir si toutes les formes de parodontite ont une influence délétère sur les thérapeutiques implantaires. Nous avons schématiquement 2 grands types de parodontite avec 90% environ de parodontites dites chroniques d’évolution relativement lente et 10% de parodontites agressives de l’adulte jeune et d’évolution rapide. De façon très schématique on considère que les parodontites chroniques sont liées à une mauvaise hygiène bucco-dentaire, une accumulation de plaque de tartre. En l’absence de traitement adéquat, l’inflammation chronique conduit à une alvéolyse progressive d’évolution lente et par palier, en fonction de l’état général. Les parodontites agressives sont de nature différente car elles touchent des individus plus jeunes et répondent d’une part à des germes beaucoup plus pathogènes, associés à une réponse immunitaire « inadaptée » (excès d’inflammation, défaut dans la chimiotaxie des neutrophiles etc ..). Afin d’apporter une réponse appropriée à la question précédemment posée il convient de regarder la littérature.
De nombreuses études vont dans le même sens depuis les années 2003 (Baelum et coll. 2004 ; Van der Weijden et coll. 2005) pour démontrer un risque accru vis-à-vis des implants avec des antécédents de parodontite. Rocusso et coll. en 2010 trouvent 10% de risque implantaire en plus chez des patients avec des antécédents de parodontites. Rinke et coll. en 2011 et l’étude française de Simonis et coll. en 2010 confirment et précisent également un risque accru chez les fumeurs. Dans une revue systématique de 5 à 10 ans Levine et coll. en 2011 montrent un taux d’échec de 5 à 6 % chez des patients sains ou avec parodontite modérée et de 12% sur des patients avec parodontites sévères.
Dans une étude de Pjetursson et coll. en 2012, les résultats révèlent de 8 à 22% de péri-implantites chez des patients avec des antécédents de parodontite. Les poches ≥ 5 mm entrainent un risque important de péri-implantite. Sur 70 patients, 38,6% ont 1 implant ou plus atteint de péri-implantite !! (Peri-implantitis susceptibility as it relates to periodontal therapy and supportive care. Pjetursson et coll. 2012). Bien entendu quelques études ne retrouvent pas ces résultats mais elles sont plus anciennes et minoritaires (Wennstrom et coll. 2004). Il semble donc que les parodontites modérées soient proches du parodonte sain en termes de risque vis-à-vis des implants, à la condition d’avoir été traitées, mais pour les parodontites sévères, le risque est augmenté de 10 à 20%.
En est-il de même pour les parodontites agressives ?
Pour ce type de parodontites les études sont beaucoup moins nombreuses et il faut bien préciser que la stabilité parodontale est possible à long terme, après traitement mécanique et/ou chirurgical et antibiothérapie systémique. (stabilisation dans 94,6% des cas, dégradation de 5,6 % à 6 mois et de 2,2% à 5 ans. Buchman et coll. 2002).

Dans une étude comparative entre parodontite chronique et parodontite agressive Heitz-Mayfeld et Lang en 2010 trouvent une progression plus rapide de la mucosite et des péri-implantites chez des patients avec des antécédents de parodontite agressive. Dans une étude à long terme de 3 à 16 ans sur des patients avec parodontite agressive généralisée (PAG) traitée, ayant reçu des implants, Swierkot et coll. 2012 retrouvent un taux de survie* de 100% chez les patients sains et de 96 % chez les patients PAG, par contre, ce qui beaucoup plus significatif, le taux de succès* est de 33% chez les patients PAG contre 50% chez ceux indemnes de parodontite. Chez les patients PAG il y a 56% de mucosite versus 40% chez les patients sains. De même il y a 26% de péri-implantite chez les patients PAG contre 10% chez les sains.
En conclusion il semble donc que le risque soit plus important pour les parodontites agressives et, de ce point de vue, la maintenance implantaire chez ces patients doit être rapprochée et particulièrement méticuleuse.
Comment se déroule une séance de maintenance professionnelle ?
Avant toute séance de contrôle, il faut penser à l’état de santé du patient. En effet, beaucoup d’éléments interviennent sur la santé de l’os et des tissus mous sans que nous pensions à les évaluer. Il faut faire un point régulier sur les traitements en cours, les interventions subies, les régimes adoptés et ne pas se contenter d’un questionnaire de santé rempli une fois pour toutes et plus jamais actualisé.
Qui sait que plus de 80 % des Français sont carencés en Vitamine D alors que cette carence est associée à une perte d’attache parodontale ? Qui tient compte d’une bonne supplémentation en vitamine D pour contribuer à diminuer la résorption osseuse ? L’évaluation de cette vitamine est impérative sous nos latitudes pour un meilleur contrôle de l’état de santé de nos patients. L’Institut de veille sanitaire (Bulletin épidémiologique, juin 2012) et l’Académie Nationale de Médecine (Bulletin de mai 2012) ont déjà adressé des prescriptions en ce sens.
L’intolérance au gluten qui concernerait 20 % des adultes, expose davantage aux phénomènes inflammatoires. Les régimes végétariens et véganes peuvent entraîner des diètes en nutriments en vitamines alors que nos traitements chirurgicaux vont demander un accroissement de la demande calorique pouvant atteindre 25 %. Il est aujourd’hui de plus en plus évident qu’il faut mettre en place, pour chaque patient, une supplémentation systématique, particulièrement chez les patients de plus de 60 ans et à fortiori en saison hivernale.
Que faudra-t-il contrôler ?
En premier lieu, le contrôle de plaque général et ensuite, l’état de la gencive péri-implantaire. La sonde parodontale est indispensable pour mesurer la profondeur du sillon péri-implantaire. Encore faut-il savoir que cette mesure n’a de valeur que par rapport à celle effectuée lors de la pose de la prothèse. A cet instant, 3 ou 4 ou 5 mm de profondeur seront mesurés et notés comme la norme à partir de laquelle les futures mesures seront comparées. Dès lors, ce contrôle aura un sens diagnostic réel car les autres symptômes comme le saignement au sondage ou la suppuration sont les signes d’une inflammation plus avancée qui nécessite la mise en œuvre de moyens plus importants.
La prévention de la péri-implantite commence donc par la gestion de l’inflammation initiale que représente la mucosite. A ce stade, pas de perte osseuse mais un contexte inflammatoire réversible à la condition d’une prise en charge efficace. Faudra-t-il passer l’aéropolisseur pour nettoyer en profondeur les piliers ? Les bains de bouche sont-ils efficaces ou faut-il leur préférer le jet dentaire ? A quelle fréquence doit-on revoir les patients en contrôle ? Autant de questions auxquelles des réponses claires et argumentées existent.

L’aéropolisseur n’est efficace que si les spires de l’implant sont visibles et un lambeau d’accès sera indiqué pour un meilleur accès. Une poudre sans bicarbonate de sodium s’impose faute de devoir passer le titane à l’acide citrique à 30 % pendant 2 minutes, pour éliminer les résidus de poudre. Les poudres à base de glycine seront donc privilégiées. Les irrigations sont plus efficaces que les bains de bouche et les antiseptiques aux huiles essentielles ou à base de polyvidone iodée (Betadine®) ont montré de meilleurs résultats que la Chlorhexidine (inactivée en sous gingival par le pus ou le sang). L’hydropulseur avec un choix d’embouts adaptés (Water Pik ®) et avec une intensité modérée pour ne pas risquer de décoller la gencive péri-implantaire s’impose à chaque porteur d’implants, pour un usage quotidien, en complément de la brosse et des brossettes.
Il faut contrôler également l’occlusion car si les implants ostéointégrés sont parfaitement « rigides dans l’os », les dents naturelles antagonistes peuvent se déplacer tout au long de la vie, même de façon minime, et ainsi modifier l’occlusion. On assiste dans certains cas heureusement rares, à une perte d’ostéointégration sans péri-implantite (sans alvéolyse) mais qui aboutissent à la dépose de l’implant.
Un contrôle annuel chez un patient sans facteur de risque sera adapté. A l’inverse, un terrain paro chez un patient fumeur imposera un contrôle tous les 3 mois, faute de quoi, la pérennité de l’implant ne pourra pas être assurée.
On voit bien qu'il y a là un problème sérieux de formation professionnelle. On comprend bien pourquoi les praticiens s'adonnent tous ensemble à la pose d'implants. Les conditions économiques des années 2010 les y ont invités. Malheureusement, en termes de qualification, le compte n'y est pas. Peu ou pas de formation universitaire, peu ou pas de compagnonnage et beaucoup de praticiens ignorants des risques et de la gestion des échecs. Aujourd’hui, la nouvelle concurrence des centres de santé impose d’accroître la production des cabinets pour faire face à l’augmentation des charges mais sans pouvoir augmenter nos honoraires. Apparaît donc un nivellement par le bas des compétences, intimement lié à l’urgence de la situation économique, associée à une offre de prix de plus en plus tirée vers le bas pour résister à cette compétition. Or, la gestion de l’acte chirurgical implantaire n’est pas tenable en deçà d’un certain budget qui inclut la responsabilité du praticien et donc le coût des suites opératoires, particulièrement en cas de péri-implantite.

La prévention de la péri-implantite passe donc par une hygiène buccale efficace. Encore faut-il que la prothèse sur implant l’autorise. Les émergences prothétiques devraient être accessibles aux outils de nettoyage. Plusieurs conseils s’imposent donc en prothèse également. Nous recommandons de réaliser chaque fois que c’est possible, des prothèses dévissables. En effet, il est plus facile de réaliser un sondage après dépose de la prothèse et c’est la meilleure façon d’éliminer tout risque de fusée de ciment dans l’espace péri-implantaire.
Il va sans dire que l’adaptation prothétique doit être satisfaisante.
Le profil d’émergence doit être conçu au laboratoire en pensant au passage des brossettes. Ni trop large pour éviter des bourrages systématiques ni trop fin, ce qui empêche tout nettoyage. Le plus simple consiste à confier des brossettes « Inava Trio compact®» jaunes, voire oranges, ce qui représente les espaces optimaux autour des implants. La présence d’une fausse gencive, le fameux « spoiler » en résine qui permet de soutenir la lèvre est une catastrophe pour l’entretien quotidien.
De plus en plus de patients expriment leur plaisir retrouvé d’avoir des dents fixes mais ils déplorent l’impossibilité de nettoyage et les problèmes d’haleine qui l’accompagne. Il est alors temps de reconsidérer la prothèse et d’adopter, par exemple, une restauration ancrée sur une barre. La satisfaction de ces patients devient maximale.

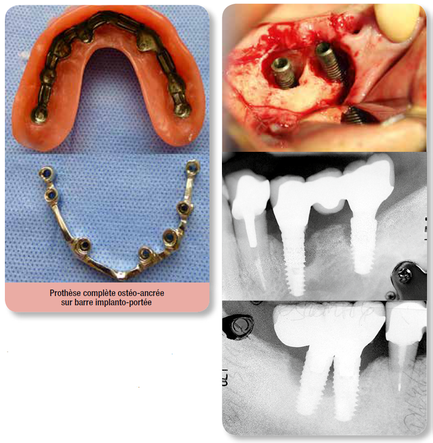
Les bridges complets sur implants doivent être réservés aux patients jeunes présentant peu de perte de volume osseux ou plus âgés mais après reconstruction préalable du volume alvéolaire. Compenser la perte de volume par de la gencive artificielle est une véritable erreur thérapeutique. Et que dire des bridges implanto-portés complets scellés sur implants avec une énorme fausse gencive, qui représentent, selon nous, la quintessence de ce qu’il ne faut jamais faire…
Voilà donc la situation telle qu’elle est. La prothèse peut également être incriminée dans le processus d’initiation d’une inflammation péri-implantaire, comme cela peut l’être autour des dents.
Il faut établir le parallèle avec le développement de la parodontologie en France dans les années 80-90-2000. Elle est balbutiante jusque dans les années 1980. Il est encore aujourd’hui bien rare de voir des bouches préparées à la chirurgie implantaire. Le simple détartrage n'est pas souvent réalisé en phase préopératoire. Dans ces conditions, comment parler de prévention de la péri-implantite. Les dentistes français ont eu du mal à intégrer le traitement parodontal à leur pratique. Ils réussissent formidablement l'intégration de la pratique implantaire, et c'est tant mieux, mais sans formation suffisante et en allant au plus court : peu ou pas de préparation initiale du patient, pas d'information sur les péri-implantites, pas de prise en charge de pathologies parodontales existantes, peu de planification prothétique pré-implantaire, peu ou pas de guide chirurgical, peu ou pas de maintenance personnalisée.
« Le périmètre du bloc opératoire permet une posture. Il ne donne pas un statut. Surtout pas celui d’implantologiste patenté. On peut être praticien averti, on peut se prétendre magicien à l’abri de conséquences mal cernées. Si poser un implant, c’est côtoyer des risques ignorés pouvant aboutir à un échec, alors il ne faut pas oublier que c’est un patient aux espoirs déçus qui subit cet échec ». J.-L. Giovannoli. Péri-implantites. Quintessence Internationale 2012.
Répétons-le, la prévention de la péri-implantite passe donc impérativement par la prise en charge de la maladie parodontale ainsi que par la prise de conscience de la part des praticiens des risques de cette maladie pour les implants mais surtout et en définitive, pour leurs patients. De plus, les conséquences de la perte d'un implant sont beaucoup plus complexes à gérerque celles de la perte d'une dent.
Pour aggraver le tout, rappelons que nous sommes dans un des rares pays développés du monde où les hygiénistes n'ont pas droit de cité. Les dentistes français n'ont pas encore tous compris que le travail en équipe est la seule façon de mettre en place une véritable politique de santé bucco-dentaire en France. Car nous n'avons que 2 mains et aucune de plus. Il y a vraiment urgence à aller de l'avant si l’on veut rester crédible. On ne peut décemment pas parler de médecine dentaire dans les congrès et séminaires de l’hexagone en restant aveugles d’une réalité incapable de donner aux Français la dentisterie dont ils devraient bénéficier.
Ceci posé, il faut savoir que les hygiénistes sont également mal à l’aise face à une perte osseuse péri-implantaire. Beaucoup n’osent pas y toucher et là encore existe un défaut patent d’information. Pour autant, ce corps de professionnels doit impérativement être mis en place dans les meilleurs délais pour être en mesure de relever le défi qui se pose à nous aujourd’hui.
Prévention, diagnostic et traitement des maladies inflammatoires implantaires et parodontales sont des étapes extrêmement chronophages pour nos agendas et il faudra pourtant les prendre en charge.
Dernier point très important : l’état de surface rugueux des implants que nous utilisons depuis plusieurs années ainsi que le protocole chirurgical choisi, enfoui ou non enfoui. D’un point de vue strictement clinique pour tous ceux qui comme nous ont commencé l’implantologie avec les implants Brånemark, le terme même de péri-implantite nous était inconnu et pendant quelques années nous étions étonnés à la lecture de certains articles qui commençaient à paraitre sur ce sujet (on parlait alors d’échec implantaire). La situation a évolué quand nous avons adopté les implants à surface rugueuse. Certes, ce type d’implant nous a fait gagner beaucoup de temps dans nos plans de traitement, on est ainsi passé de 6 mois pour la phase d’ostéointégration à 2 mois, mais avec le recul que nous avons aujourd’hui une question se pose : fallait-il prendre ce risque pour gagner 4 mois ?
En effet, quand on reprend l’ensemble des cas traités avec des surfaces usinées, les résultats dans le long terme sont exceptionnels et même parfois pour des patients fumeurs ou chez lesquels le contrôle de plaque était aléatoire. Sur des cas traités entre 15 et 20 ans avec ces surfaces usinées on observe parfois une alvéolyse de 1 à 3 ou 4 mm mais celle-ci est horizontale et ne semble entrainer aucune suppuration, tout au plus un saignement au sondage. Si on se réfère aux critères de succès de Lekholm et Zarb de 1985 ces cas correspondent bien à un succès à long terme. Par contre avec des surfaces rugueuses et pour certains patients qui ont un mauvais contrôle de plaque, l’évolution de la mucosite vers la péri-implantite peut aller très vite, avec une alvéolyse angulaire spectaculaire. Il devient alors complexe de décontaminer ces surfaces rugueuses et le traitement de cette péri-implantite est alors très difficile. Une solution pourrait être d’avoir la partie coronaire de l’implant avec une surface usinée et la partie plus apicale en surface rugueuse.
Il est toujours compliqué de revenir en arrière et de proposer à nos patients aujourd’hui d’attendre presque un an avant d’avoir leurs dents sur leurs implants mais la question se pose néanmoins, de revenir aux fondamentaux édictés par le regretté Professeur Brånemark et ce point de vue est partagé par plusieurs implantologues et non des moindres dont Paul Mattout, Jean François Tulasne et bien d’autres.
N’oublions pas que les industriels ont leur part d’engagement dans cette prévention. Comment est-il possible en 2016 de ne pas disposer d'implants à surface usinée pour les patients dits à risque ? En effet, une fois la perte osseuse installée, un col en titane rugueux est pratiquement impossible à nettoyer quotidiennement.
Chaque fabricant d’implant se doit de mettre au plus vite à notre disposition une gamme d’implant présentant un col de 3-4 mm lisse, le reste du corps restant modérément rugueux afin de pouvoir enfin adapter notre thérapeutique implantaire au profil médico dentaire du patient concerné.
Conclusions
En définitive, c'est toute l'organisation de la pratique implantaire française qu'il faut revoir si on veut reprendre en mains une situation vraiment hors de contrôle actuellement. La découverte de l’ostéointégration est un évènement majeur de l’histoire de la dentisterie. La pratique de cette implantologie moderne fût, à ses débuts, et sur les recommandations du Pr Brånemark lui-même, réservée à des praticiens parodontistes car il était alors évident qu’ils étaient les plus compétents et les mieux préparés à gérer les tissus péri-implantaires. Aujourd’hui, cette pratique s’est banalisée jusqu’à la caricature et il paraît peu probable que cela puisse continuer encore longtemps de la sorte sans avoir à en payer chèrement le prix.
C’est à chacun, dans son cabinet, de voir la réalité en face et de se demander si cela a un sens d’abandonner ses valeurs sur l’autel de la rentabilité de survie. Oui, le diagnostic et le traitement des parodontopathies est un pré-requis du traitement implantaire. Oui, le chirurgien-dentiste a un rôle à jouer vis-à-vis de l’addiction tabagique mais pas seulement. Il doit intégrer l’implant dans sa pratique en ayant été correctement formé à cela et en ayant conscience des avantages et inconvénients d’un tel traitement en fonction du profil de chaque patient. Oui, la finalité de ces thérapeutiques est de donner le meilleur des soins possibles à nos patients qui sont au cœur de nos priorités. Oui, c’est comme cela que nous marquerons notre différence avec les comportements bassement mercantiles qui caractérisent les centres de santé actuels. Enfin, c’est aux autorités de ce pays de comprendre qu’il faut faire évoluer le métier d’assistante dentaire en créant celui d’hygiéniste dentaire afin de faire face efficacement au défi de santé publique que représentera demain la péri-implantite.
C'est notre rôle en tant qu'acteur majeur de la formation continue de mettre chacun devant ses propres responsabilités en lui donnant toutes les informations qui lui manquent, à l'instant où nous parlons, et nous espérons contribuer ainsi à faire évoluer les consciences
Retour au Dossier Spécial 25 ans - AOnews #30 Novembre 2019